Baggrund
Insulin er et hormon, der regulerer mængden af glukose (sukker) i blodet, og er nødvendig for kroppen at fungere normalt. Insulin produceres af celler i bugspytkirtlen, kaldet Langerhans øer. Disse celler frigiver kontinuerligt en lille mængde insulin i kroppen, men de frigiver overspændinger af hormonet som reaktion på en stigning i blodglukoseniveauet.,
visse celler i kroppen ændrer den mad, der indtages i energi eller blodglukose, som celler kan bruge. Hver gang en person spiser, stiger blodglukosen. Forhøjet blodsukker udløser cellerne i Langerhans øer for at frigive den nødvendige mængde insulin. Insulin gør det muligt at transportere blodglukosen fra blodet ind i cellerne. Celler har en ydre væg, kaldet en membran, der styrer, hvad der kommer ind og ud af cellen. Forskere ved endnu ikke nøjagtigt, hvordan insulin fungerer, men de ved, at insulin binder sig til receptorer på cellens membran., Dette aktiverer et sæt transportmolekyler, så glukose og proteiner kan komme ind i cellen. Cellerne kan derefter bruge glukosen som energi til at udføre dens funktioner. Når det er transporteret ind i cellen, returneres blodglukoseniveauet til det normale inden for få timer.
uden insulin ophobes blodsukkeret i blodet, og cellerne sultes af deres energikilde. Nogle af de symptomer, der kan forekomme, inkluderer træthed, konstante infektioner, sløret syn i øjnene, følelsesløshed, prikken i hænder eller ben, øget tørst og nedsat heling af blå mærker eller nedskæringer., Cellerne vil begynde at bruge fedt, energikilden opbevares i nødsituationer. Når dette sker for længe, producerer kroppen ketoner, kemikalier produceret af leveren. Ketoner kan forgifte og dræbe celler, hvis de bygger sig op i kroppen over en længere periode. Dette kan føre til alvorlig sygdom og koma.
personer, der ikke producerer den nødvendige mængde insulin, har diabetes. Der er to generelle typer diabetes. Den mest alvorlige type, kendt som Type I eller juvenil diabetes, er, når kroppen ikke producerer noget insulin., Diabetikere af type i injicerer normalt sig selv med forskellige typer insulin tre til fire gange dagligt. Dosering er taget ud fra personens blodsukkeraflæsning, taget fra en glukosemåler. Type II diabetikere producerer noget insulin, men det er enten ikke nok, eller deres celler reagerer ikke normalt på insulin. Dette forekommer normalt hos overvægtige eller middelaldrende og ældre mennesker. Type II diabetikere behøver ikke nødvendigvis at tage insulin, men de kan injicere insulin en eller to gange om dagen.,
Der er fire hovedtyper af insulin fremstillet baseret på hvor hurtigt insulinet begynder at virke, når det topper, og hvor længe det varer i kroppen. Ifølge American Diabetes Association når hurtigtvirkende insulin blodet inden for 15 minutter, topper 30-90 minutter og kan vare fem timer. Kortvirkende insulin når blodet inden for 30 minutter, det topper cirka to til fire timer senere og forbliver i blodet i fire til otte timer., Mellemvirkende insulin når blodet to til seks timer efter injektion, topper fire til 14 timer senere og kan vare i blodet i 14-20 timer. Og langtidsvirkende insulin tager seks til 14 timer at begynde at arbejde, det har en lille top kort efter og forbliver i blodet i 20-24 timer. Diabetikere har hver forskellige reaktioner på og behov for insulin, så der er ingen type, der fungerer bedst for alle. Nogle insulin sælges med to af typerne blandet sammen i en flaske.,
historie
Hvis kroppen ikke producerer noget eller nok insulin, skal folk tage en fremstillet version af det. Den største anvendelse af at producere insulin er til diabetikere, der ikke fremstiller nok eller noget insulin naturligt.
før forskere opdagede, hvordan man producerer insulin, havde mennesker, der led af type i-diabetes, ingen chance for et sundt liv. Så i 1921, canadiske forskere Frederick G. Banting og Charles H. bedst med succes renset insulin fra en hunds bugspytkirtel. I årenes løb har forskere foretaget løbende forbedringer i produktionen af insulin., I 1936 fandt forskere en måde at fremstille insulin med en langsommere frigivelse i blodet. De tilføjede et protein, der findes i fiskesæd, protamin, som kroppen bryder langsomt ned. En injektion varede 36 timer. Et andet gennembrud kom i 1950, da forskere producerede en type insulin, der handlede lidt hurtigere og ikke forbliver i blodbanen så længe. I 1970 ‘ erne begyndte forskere at forsøge at producere et insulin, der mere efterlignede, hvordan kroppens naturlige insulin fungerede: frigivelse af en lille mængde insulin hele dagen med stigninger, der forekom ved måltiderne.,
forskere fortsatte med at forbedre insulin, men den grundlæggende produktionsmetode forblev den samme i årtier. Insulin blev ekstraheret fra bugspytkirtlen hos kvæg og svin og renset. Den kemiske struktur af insulin i disse dyr er kun lidt anderledes end humant insulin, hvorfor det fungerer så godt i menneskekroppen. (Selvom nogle mennesker havde negativt immunsystem eller allergiske reaktioner.) I begyndelsen af 1980 ‘ erne revolutionerede bioteknologien insulinsyntese. Forskere havde allerede afkodet den kemiske struktur af insulin i midten1950 ‘ erne., De bestemte snart den nøjagtige placering af insulingenet øverst på kromosom 11. I 1977 havde et forskerteam splejset et rotteinsulingen i en bakterie, der derefter producerede insulin.

i 1891 blev Frederick Banting født i Alliston, Ontario. Han uddannede sig i 1916 fra University of Toronto medical school. Efter Medical Corps service i Første Verdenskrig blev Banting interesseret i diabetes og studerede sygdommen ved University of Westernestern Ontario.,
i 1919 viste Moses Barron, en forsker ved University of Minnesota, blokering af kanalen, der forbinder de to hoveddele af bugspytkirtlen, forårsaget krympning af en anden celletype, acinaren. Banting mente, at ved at binde bugspytkirtelkanalen for at ødelægge acinarcellerne, kunne han bevare hormonet og ekstrahere det fra holmceller. Banting foreslog dette til lederen af University of Torontos Fysiologiafdeling, John Macleod., Macleod afvist Banting ‘ s forslag, men leveres laboratorium plads, 10 hunde, og en medicinsk student, Charles Best
Starter i Maj 1921, Banting og Best bundet pancreas kanaler i hunde, så de acinar celler ville atrofi, så fjernet pancreases til at udtrække væske fra holmen celler. I mellemtiden fjernede de bugspytkirtler fra andre hunde for at forårsage diabetes og injicerede derefter øcellevæsken. I januar 1922 blev 14-årige Leonard Thompson det første menneske, der med succes blev behandlet for diabetes ved hjælp af insulin.
Best modtog sin medicinske grad i 1925., Banting insisterede bedst også blive krediteret, og næsten afvist hans Nobelpris, fordi Best ikke var inkluderet. Bedste blev leder af University of Toronto ‘s fysiologi afdeling i 1929 og direktør for universitetets Banting og Best Institut for Medicinsk Forskning efter Banting’ s død i 1941.
i 1980 ‘ erne brugte forskere genteknologi til at fremstille et humant insulin. I 1982 producerede Eli Lilly Corporation et humant insulin, der blev det første godkendte genetisk manipulerede farmaceutiske produkt., Uden at skulle være afhængig af dyr, kunne forskere producere genetisk manipuleret insulin i ubegrænsede forsyninger. Det indeholdt heller ikke nogen af de animalske forurenende stoffer. Brug af humant insulin fjernede også eventuelle betænkeligheder ved at overføre potentielle dyresygdomme til insulinet. Mens virksomheder stadig sælger en lille mængde insulin produceret fra dyr—for det meste svin-fra 1980 ‘ erne og fremefter, flyttede insulinbrugere i stigende grad til en form for humant insulin skabt ved hjælp af rekombinant DNA-teknologi., Ifølge Eli Lilly Corporation, i 2001 95% af insulinbrugere i de fleste dele af verden tage en form for humant insulin. Nogle virksomheder er stoppet med at producere animalsk insulin fuldstændigt. Virksomheder fokuserer på at syntetisere humane insulin-og insulinanaloger, en ændring af insulinmolekylet på en eller anden måde.
råvarer
humant insulin dyrkes i laboratoriet inde i almindelige bakterier. Escherichia coli er langt den mest anvendte type bakterie, men gær bruges også.
forskere har brug for det humane protein, der producerer insulin., Producenter får dette gennem en aminosyre-sekventeringsmaskine, der syntetiserer DNA ‘ et. Producenter kender den nøjagtige rækkefølge af insulinets aminosyrer (de nitrogenbaserede molekyler, der stiller op til at udgøre proteiner). Der er 20 almindelige aminosyrer. Producenter input insulin aminosyrer, og sekventering maskine forbinder aminosyrerne sammen. Også nødvendigt at syntetisere insulin er store tanke til at dyrke bakterierne, og næringsstoffer er nødvendige for bakterierne at vokse., Flere instrumenter er nødvendige for at adskille og rense DNA ‘ et, såsom en centrifuge, sammen med forskellige kromatografi-og røntgenkrystallografiinstrumenter.
fremstillingsprocessen
syntetisering af humant insulin er en biokemisk proces i flere trin, der afhænger af grundlæggende rekombinante DNA-teknikker og en forståelse af insulingenet. DNA bærer instruktionerne for, hvordan kroppen fungerer, og et lille segment af DNA ‘ et, insulingenet, koder for proteininsulinet. Producenter manipulerer den biologiske forløber for insulin, så den vokser inde i enkle bakterier., Mens producenterne hver har deres egne variationer, er der to grundlæggende metoder til fremstilling af humant insulin.
arbejde med humant insulin
- 1 insulingenet er et protein bestående af to separate kæder af aminosyrer, en A over en B-kæde, der holdes sammen med bindinger. Aminosyrer er de grundlæggende enheder, der bygger alle proteiner. Insulin a-kæden består af 21 aminosyrer og B-kæden har 30.
- 2 før insulin bliver et aktivt insulinprotein, produceres insulin først som preproinsulin., Dette er en enkelt lang proteinkæde med A-og B-kæderne, der endnu ikke er adskilt, et afsnit i midten, der forbinder kæderne sammen og en signalsekvens i den ene ende, der fortæller proteinet, hvornår man skal begynde at udskille uden for cellen. Efter preproinsulin Udvikler kæden sig til proinsulin, stadig en enkelt kæde, men uden signalsekvensen. Derefter kommer det aktive proteininsulin, proteinet uden sektionen, der forbinder A-og B-kæderne. Ved hvert trin har proteinet specifikke en .ymer (proteiner, der udfører kemiske reaktioner) for at producere den næste form for insulin.,
startende med A og B
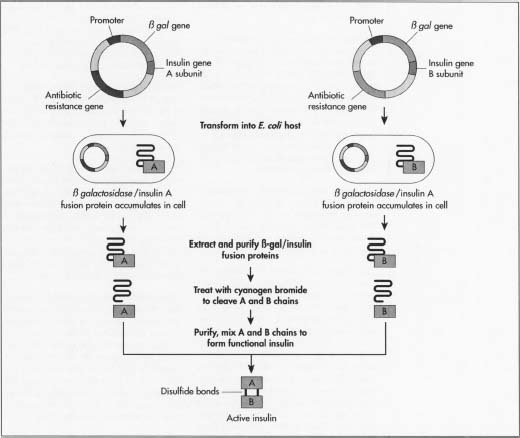
- 3 en metode til fremstilling af insulin er at dyrke de to insulinkæder separat. Dette vil undgå fremstilling af hvert af de specifikke en .ymer, der er nødvendige. Producenter har brug for de to mini-gener: en, der producerer a-kæden og en til b-kæden. Da den nøjagtige DNA-sekvens af hver kæde er kendt, syntetiserer de hvert mini-gens DNA i en aminosyresekventeringsmaskine.
- 4 disse to DNA-molekyler indsættes derefter i plasmider, små cirkulære stykker DNA, der lettere optages af værtsens DNA., 5 producenter indsætter først plasmiderne i en ikke-skadelig type af bakterien E. coli. De indsætter det ved siden af Lac. – genet. Lac.koder for 8-galactosidase, et gen, der i vid udstrækning anvendes i rekombinante DNA-procedurer, fordi det er let at finde og skære, hvilket gør det muligt at fjerne insulinet let, så det ikke går tabt i bakteriens DNA. Ved siden af dette gen er aminosyren methionin, som starter proteindannelsen.
- 6 de rekombinante, nydannede plasmider blandes med bakteriecellerne. Plasmider kommer ind i bakterierne i en proces kaldet transfektion., Producenter kan tilføje til cellerne DNA-ligase, et en .ym, der fungerer som lim for at hjælpe plasmidet med at holde sig til bakteriens DNA.
- 7 bakterierne, der syntetiserer insulinet, gennemgår derefter en fermenteringsproces. De dyrkes ved optimale temperaturer i store tanke i produktionsanlæg. Millioner af bakterier replikerer omtrent hvert 20. minut gennem cellemitose, og hver udtrykker insulingenet.
- 8 efter multiplikation tages cellerne ud af tanke og brydes åbent for at ekstrahere DNA ‘ et., En almindelig måde, dette gøres på, er ved først at tilsætte en blanding af Lyso .om, der fordøjer det ydre lag af cellevæggen, og derefter tilsætte en vaskemiddelblanding, der adskiller fedtcellevægsmembranen. Bakteriens DNA behandles derefter med cyanogenbromid, et reagens, der opdeler proteinkæder ved methioninresterne. Dette adskiller insulinkæderne fra resten af DNA ‘ et.
- 9 de to kæder blandes derefter sammen og forbindes af disulfidbindinger gennem reduktionsreo .idationsreaktionen. Et O .idationsmiddel (et materiale, der forårsager o .idation eller overførsel af en elektron) tilsættes., Batchet placeres derefter i en centrifuge, en mekanisk enhed, der hurtigt spinder for at adskille cellekomponenter efter størrelse og densitet.
- 10 DNA-blandingen renses derefter, så kun insulinkæderne forbliver. Producenter kan rense blandingen gennem flere kromatografi, eller adskillelse, teknikker, der udnytter forskelle i molekylets ladning, størrelse, og affinitet til vand. De anvendte procedurer omfatter en ionbytterkolonne, reversfaset højtydende væskekromatografi og en gelfiltreringskromatografisøjle., Producenter kan teste insulinbatcher for at sikre, at ingen af bakteriens E. coli-proteiner blandes med insulinet. De bruger et markørprotein, der lader dem opdage E. coli-DNA. De kan derefter bestemme, at rensningsprocessen fjerner E. coli-bakterierne.
PROINSULINPROCES
- 11 fra 1986 begyndte producenterne at bruge en anden metode til at syntetisere humant insulin. De startede med den direkte forløber for insulingenet, proinsulin., Mange af trinnene er de samme som ved fremstilling af insulin med A-og B-kæderne, undtagen i denne metode syntetiserer aminosyremaskinen proinsulingenet. 12 den sekvens, der koder for proinsulin, indsættes i de ikke-patogene E. coli-bakterier. Bakterierne går gennem fermenteringsprocessen, hvor den reproducerer og producerer proinsulin. Derefter splejses forbindelsessekvensen mellem A-og B-kæderne væk med et en .ym, og det resulterende insulin renses.,
- 13 Ved afslutningen af fremstillingsprocessen tilsættes ingredienser til insulin for at forhindre bakterier og hjælpe med at opretholde en neutral balance mellem syrer og baser. Ingredienser tilsættes også til mellemliggende og langtidsvirkende insulin for at producere den ønskede varighed type insulin. Dette er den traditionelle metode til fremstilling af længerevirkende insulin. Producenter tilføjer ingredienser til det rensede insulin, der forlænger deres handlinger, såsom .inko .id. Disse tilsætningsstoffer forsinker absorption i kroppen. Tilsætningsstoffer varierer mellem forskellige mærker af samme type insulin.,
Analog insulin
I midten af 1990’erne, forskere begyndte at forbedre den måde, human insulin virker i kroppen ved at ændre dets aminosyre sekvens og skabe en analog, et kemisk stof, der efterligner et andet stof godt nok til, at det fjolser cellen. Analog insulin klumper mindre og spredes lettere i blodet, så insulinet kan begynde at arbejde i kroppen minutter efter en injektion. Der er flere forskellige analoge insulin. Humulin insulin har ikke stærke bindinger med andet insulin og absorberes således hurtigt., En anden insulinanalog, kaldet glargin, ændrer proteinets kemiske struktur for at få det til at få en relativt konstant frigivelse over 24 timer uden udtalt toppe.
i stedet for at syntetisere den nøjagtige DNA-sekvens for insulin syntetiserer producenter et insulingen, hvor sekvensen ændres lidt. Ændringen medfører den resulterende
proteiner til at afvise hinanden, hvilket forårsager mindre klumpning., Ved hjælp af denne ændrede DNA-sekvens svarer fremstillingsprocessen til den beskrevne rekombinante DNA-proces.
kvalitetskontrol
efter syntetisering af det humane insulin testes strukturen og renheden af insulinbatchene ved hjælp af flere forskellige metoder. Højtydende væskekromatografi bruges til at bestemme, om der er urenheder i insulinet. Andre separationsteknikker, såsom røntgenkrystallografi, gelfiltrering og aminosyresekvensering, udføres også. Fabrikanter tester også hætteglassets emballage for at sikre, at den er forseglet korrekt.,
fremstilling af humant insulin skal overholde National Institutes of Health procedures for large-scale operations. USA ‘ s Food and Drug Administration skal godkende alt fremstillet insulin.
fremtiden
fremtiden for insulin har mange muligheder. Da insulin først blev syntetiseret, havde diabetikere brug for regelmæssigt at injicere det flydende insulin med en sprøjte direkte i deres blodbanen. Dette gør det muligt for insulin at komme ind i blodet med det samme. I mange år var det den eneste måde kendt at flytte det intakte insulinprotein ind i kroppen., I 1990 ‘ erne begyndte forskere at gøre indhug i syntetisering af forskellige enheder og former for insulin, som diabetikere kan bruge i et alternativt lægemiddelleveringssystem.
producenter producerer i øjeblikket flere relativt nye lægemidler. Insulinpenne ligner en skrivepen. Cylinderampullen holder insulinet, og spidsen er nålen. Brugeren indstiller en dosis, indsætter nålen i huden og trykker på en knap for at injicere insulinet. Med penne er det ikke nødvendigt at bruge et hætteglas med insulin. Penne skal dog indsættes separate spidser før hver injektion., En anden ulempe er, at pennen ikke tillader brugere at blande insulintyper, og ikke alt insulin er tilgængeligt.
for personer, der hader nåle, er en alternativ til pennen jet-injektoren. Ligner pennene, bruger jetinjektorer tryk for at drive en lille strøm af insulin gennem huden. Disse enheder er ikke så udbredt som pennen, og de kan forårsage blå mærker ved indgangspunktet.
insulinpumpen muliggør kontrolleret frigivelse i kroppen. Dette er en computeriseret pumpe, på størrelse med en bipper, som diabetikere kan bære på deres bælte eller i lommen., Pumpen har et lille fleksibelt rør, der indsættes lige under overfladen af diabetikerens hud. Diabetikeren sætter pumpen til at levere en stabil, målt dosis insulin hele dagen, hvilket øger mængden lige før du spiser. Dette efterligner kroppens normale frigivelse af insulin. Producenter har produceret insulinpumper siden 1980 ‘erne, men fremskridt i slutningen af 1990’ erne og begyndelsen af det enogtyvende århundrede har gjort dem stadig lettere at bruge og mere populære. Forskere undersøger muligheden for implanterbare insulinpumper., Diabetikere ville kontrollere disse enheder via en ekstern fjernbetjening.
forskere undersøger andre lægemiddelleveringsmuligheder. Indtagelse af insulin gennem piller er en mulighed. Udfordringen med spiseligt insulin er, at mavens høje sure miljø ødelægger proteinet, før det kan bevæge sig ind i blodet. Forskere arbejder på at belægge insulin med plast bredden af et par menneskelige hår. Belægningerne ville beskytte stofferne mod mavesyren.,
i 2001 forekommer lovende test på inhalerede insulinapparater, og producenterne kunne begynde at producere produkterne inden for de næste par år. Da insulin er et relativt stort protein, gennemsyrer det ikke i lungerne. Forskere af inhaleret insulin arbejder på at skabe insulinpartikler, der er små nok til at nå den dybe lunge. Partiklerne kan derefter passere ind i blodbanen. Forskere tester flere inhalationsanordninger, der ligner en astmainhalator.
en anden form for aerosolanordning, der gennemgår test, administrerer insulin til den indre kind., Kendt som buccal (kind) insulin, vil diabetikere sprøjte insulin på indersiden af deres kind. Det absorberes derefter gennem den indre kindvæg.
Insulinplaster er et andet lægemiddelleveringssystem under udvikling. Patches ville frigive insulin kontinuerligt i blodbanen. Brugere ville trække en fane på plasteret for at frigive mere insulin før måltider. Udfordringen er at finde en måde at få insulin til at passere gennem huden. Ultralyd er en metode forskere undersøger. Disse lavfrekvente lydbølger kan ændre hudens permeabilitet og tillade insulin at passere.,
anden forskning har potentialet til at afbryde behovet for, at producenter syntetiserer insulin. Forskere arbejder på at skabe de celler, der producerer insulin i laboratoriet. Tanken er, at læger en dag kan erstatte de ikke-arbejdende bugspytkirtelceller med insulinproducerende celler. Et andet håb for diabetikere er genterapi. Forskere arbejder på at korrigere insulingenets mutation, så diabetikere ville være i stand til at producere insulin alene.
M. Rae Nelson
Skriv et svar