¿qué es la homeopatía?
La homeopatía es una práctica médica alternativa que se desarrolló a finales de 1700. La homeopatía generalmente se basa en dos principios principales:
- que una sustancia que causa síntomas en una persona sana puede usarse en forma diluida para tratar síntomas y enfermedades, un principio conocido como «similar-cura-similar»; y
- cuanto más diluida es la sustancia, más potente es, que se conoce como la «Ley de infinitesimales».,»
históricamente, los productos homeopáticos se han identificado a través de» pruebas», en las que se administran sustancias a voluntarios sanos en concentraciones que causan síntomas. Los síntomas experimentados por los voluntarios se registran para indicar posibles usos terapéuticos de las sustancias. En otras palabras, si una sustancia causa un síntoma particular, las personas que experimentan ese síntoma serían tratadas con una solución diluida hecha de esa sustancia.
¿qué son los productos homeopáticos y cómo puede saber que está tomando uno?,
no hay productos aprobados por la FDA etiquetados como homeopáticos; esto significa que cualquier producto etiquetado como homeopático se comercializa en los EE. Estos productos a menudo se comercializan como alternativas naturales, seguras y efectivas a los productos aprobados con y sin receta, y se venden en línea y en las principales tiendas minoristas.
Los Productos etiquetados como homeopáticos pueden contener una amplia gama de sustancias, incluidos ingredientes derivados de plantas, fuentes animales o humanas sanas o enfermas, minerales y productos químicos.,
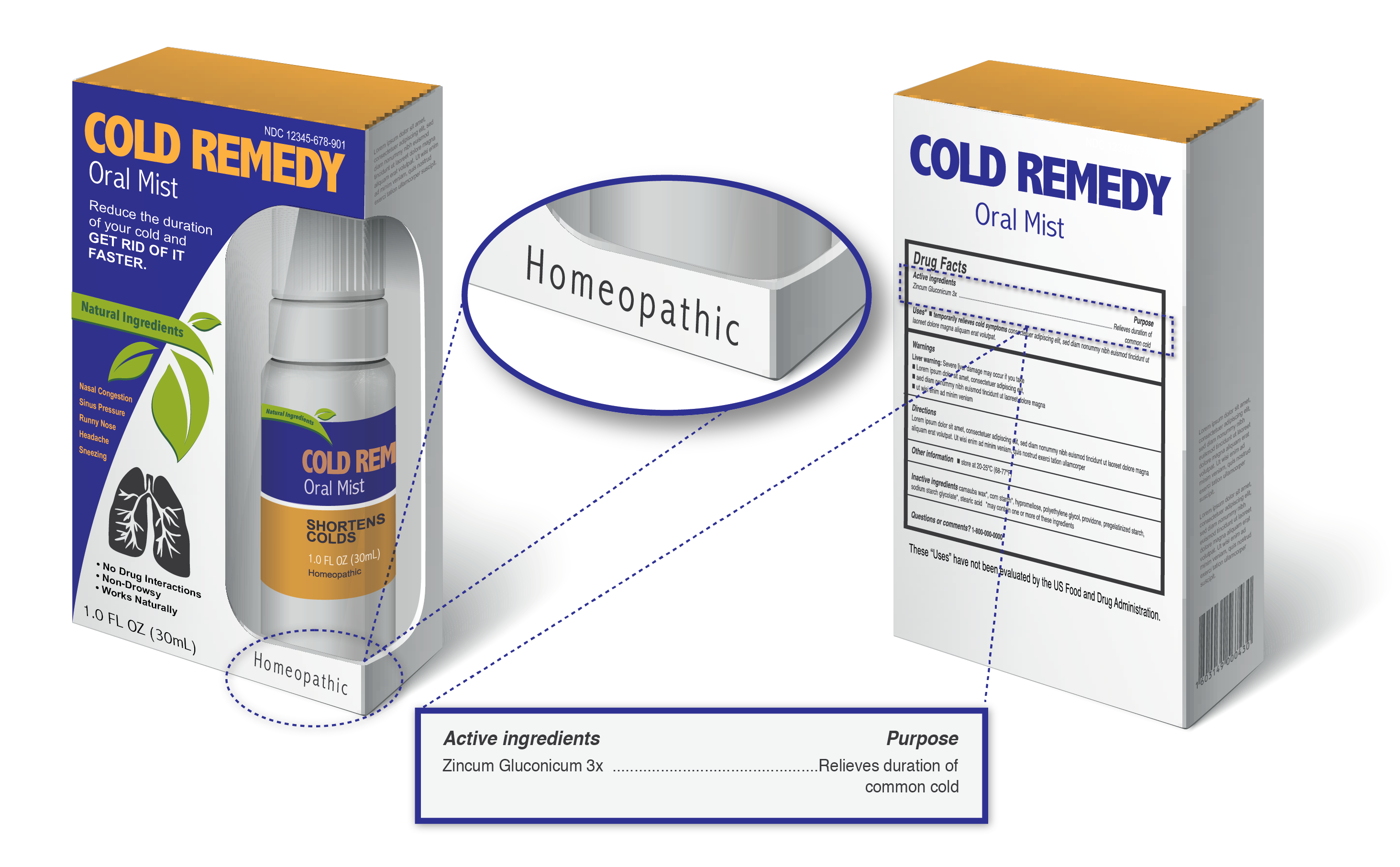
Los Productos etiquetados como homeopáticos generalmente incluyen:
- La palabra «homeopático»
- Los ingredientes enumerados en términos de dilución, por ejemplo, 1X, 6X, 2C
volver al principio
¿está preocupada la FDA por la seguridad de los productos homeopáticos?
mientras que los productos etiquetados como homeopáticos generalmente se etiquetan como altamente diluidos, se ha encontrado que algunos de estos productos contienen cantidades mensurables de ingredientes activos y, por lo tanto, podrían causar un daño significativo al paciente., Además, la FDA ha probado productos que se fabricaron incorrectamente, lo que puede causar diluciones incorrectas y aumentar el potencial de contaminación. Además, algunos productos etiquetados como homeopáticos se comercializan para tratar enfermedades o afecciones graves.,nWide recall of homeopathic water-based medicines due to microbial contamination
¿qué deben saber los consumidores sobre los productos homeopáticos?,
Los Productos etiquetados como homeopáticos y comercializados actualmente en los Estados Unidos no han sido revisados por la FDA en cuanto a su seguridad y efectividad para diagnosticar, tratar, curar, prevenir o mitigar cualquier enfermedad o condición. Las revisiones de medicamentos basadas en evidencia de la FDA desempeñan un papel esencial para garantizar que los medicamentos se fabrican con procesos de fabricación de calidad y son seguros y efectivos para los usos previstos., Los productos que no han sido evaluados para su seguridad y efectividad pueden dañar a los consumidores que eligen tratar enfermedades o afecciones graves con dichos productos, y los consumidores pueden estar renunciando al tratamiento con un producto médico que se ha demostrado científicamente que es Seguro y efectivo.
LA FDA recomienda a los consumidores que hablen con su médico o profesional de la salud sobre tratamientos seguros y eficaces para su enfermedad o afección.
volver al principio
¿cómo se regulan los productos homeopáticos?,
bajo la Ley Federal de Alimentos, Medicamentos y cosméticos, los productos homeopáticos están sujetos a los mismos requisitos relacionados con la aprobación, adulteración y etiquetado incorrecto que otros productos farmacéuticos. Actualmente no hay productos homeopáticos aprobados por la FDA.
en 1988, la FDA emitió la Guía de políticas de cumplimiento (CPG) 400.400, titulada «condiciones bajo las cuales se pueden comercializar medicamentos homeopáticos», que describía la política de cumplimiento de la agencia. El 24 de octubre de 2019, la FDA retiró la CPG 400.400 porque es inconsistente con nuestro enfoque basado en el riesgo para las medidas regulatorias y de cumplimiento., La FDA también emitió un borrador revisado de guía: productos farmacéuticos etiquetados como homeopáticos, para comentarios públicos. Dado que los medicamentos homeopáticos no han sido aprobados por la FDA para ningún uso, es posible que no cumplan con los estándares modernos de seguridad, eficacia y calidad.
este borrador de guía revisado propone un enfoque integral de cumplimiento basado en el riesgo para los productos homeopáticos comercializados sin la aprobación de la FDA.
el enfoque propuesto por la FDA prioriza las acciones regulatorias y de cumplimiento que involucran productos homeopáticos no aprobados que representan el mayor riesgo para los pacientes., Muchos productos homeopáticos probablemente caerán fuera de las categorías basadas en el riesgo descritas en el borrador revisado de la guía. La FDA tiene la intención de centrar sus autoridades de aplicación en los siguientes tipos de productos:
- Con preocupaciones de seguridad reportadas;
- que contienen o pretenden contener ingredientes asociados con preocupaciones de seguridad potencialmente significativas;
- Para vías de administración que no sean orales o tópicas, P., para su uso como inyección o por vía nasal;
- que afirman tratar o prevenir enfermedades y afecciones graves y/o que ponen en peligro la vida, como el cáncer;
- comercializado para poblaciones vulnerables, incluidos niños, mujeres embarazadas y ancianos; o
- con problemas de calidad significativos.
¿la FDA va a eliminar los productos homeopáticos del mercado?
la principal preocupación de la FDA es la seguridad del paciente. Cuando se finalice el proyecto de orientación, se especificarán las categorías de productos que el organismo se propone priorizar para su aplicación., Mientras tanto, antes de que se finalice el proyecto de directrices, la dirección de Desarrollo Forestal tiene la intención de aplicar su enfoque general para dar prioridad a las medidas reglamentarias y de aplicación de la ley basadas en el riesgo.
Deja una respuesta