Paine ja KMT
makroskooppiset ilmiöt paine voidaan selittää kannalta molekyyli-kineettinen teoria kaasuja. Oletetaan tapaus, jossa kaasumolekyyli (jota edustaa pallo) on laatikossa, pituus L (kuva 1). Kautta käyttäen oletuksia säädettyihin edellä, ja kun otetaan huomioon, että alalla on vain liikkuu x-suuntaan, voimme tutkia esimerkiksi pallo törmää elastisesti, jossa yksi seinä laatikon.,
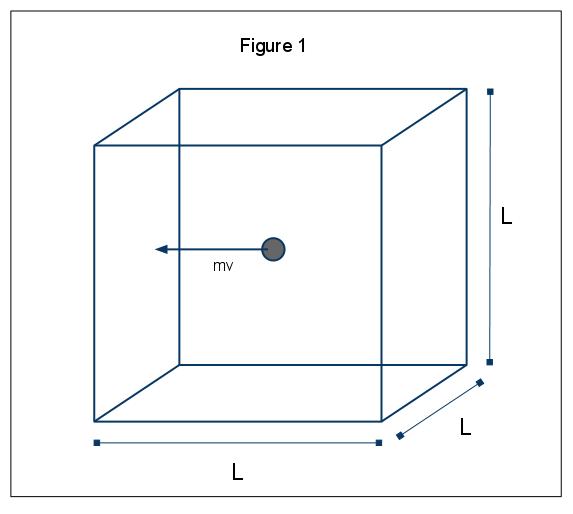
vauhtia tämä törmäys on antanut p=mv, tässä tapauksessa p=mvx, koska olemme vain ottaen huomioon, x-ulottuvuus. Yhteensä liikemäärän muutos törmäyksessä on sitten antama
\
ottaen Huomioon, että paljon aikaa se kestää törmäykset molekyylin kanssa seinä on L/vx voimme antaa taajuus törmäykset molekyylin vastaan tietyn seinän box-yksikköä kohti aikaa, kuten vx/2L., Yksi voi nyt ratkaista, jotta muutos vauhtia aikayksikköä kohti:
\
Ratkaiseminen vauhtia aikayksikössä antaa kohdistama esine (F=ma=p/kerta)., Kanssa, että lauseke F=mvx2/L voidaan nyt ratkaista painostus molekyylien törmäys, jossa alue annetaan alueen yhden seinän laatikko, A=L2:
\
\
lauseke voidaan nyt kirjoitettu ehdot paine liittyvät törmäykset N määrä molekyylejä:
\
Tämä lauseke voidaan nyt säätää tilin liikkeen x -, y-ja z-suuntiin käyttämällä mean-square velocity kolme ulottuvuutta ja suuri arvo N., Ilme nyt on kirjoitettu seuraavasti:
\
Tämä ilmaus nyt antaa painetta, makroskooppinen laadun kannalta atomic motion. Merkitys edellä suhde on, että paine on verrannollinen mean-square nopeus molekyylien tietyssä astiassa. Siksi molekyylin nopeuden kasvaessa myös säiliöön kohdistuva paine kasvaa.
Vastaa