Johdanto
Posterior virtsaputken venttiilit (PUV) on yleisin synnynnäinen syy lasten virtsarakon pistorasiaan tukkeuma (1). Vaikka kuolleisuus PUV on merkittävästi parantunut, joissa on moderni lääketieteellinen hoito, obstruktiivinen uropathy edelleen merkittävää sairastuvuutta aikuisuuteen (2). Jopa 80%: lla PUV-lapsista esiintyy inkontinenssin ja virtsatieinfektioiden oireita (3)., Lisäksi, jopa 50% lapsista PUV kehittää munuaisten vajaatoiminta, joilla on obstruktiivinen uropathy yleisin synnynnäinen syy munuaisensiirron jälkeen (4). Obstruktiivinen venttiili esitteet kirurgisesti hoidetaan pian syntymän jälkeen; kuitenkin, lapset PUV kehittää vaihtelua virtsarakon toiminta koko elämänsä. On osoitettu, että virtsarakon heikkeneminen tapahtuu usein seuraavat murrosikä, kanssa kasvava tarve ajoittainen puhdas katetrointi (5).
eri eläinmalleja hyödyntävät tutkimukset ovat osoittaneet rakon olevan hormonaalisesti herkkä., Erityisesti testosteronikorvaushoitoa on osoitettu lisäävän sileän lihaksen massa, ja sileä lihas kollageenin suhde orchiectomized rotilla (6). Malli osittainen virtsarakon pistorasiaan tukkeuma uroshiirillä oli tutkittu ja osoitettu tuottaa virtsarakon tyhjentäjälihaksen lihas liikakasvu (7). Testosteronin on osoitettu lisäävän detrusor–fibroosia kastroitujen kanien iskemian ja reperfuusiovaurion vasteena (8). Kuitenkin, tähän mennessä, vaikutus hormonaalista manipulointi vastaus uros hiiri virtsarakon vahinkoa valmistettu tukos ei ole vielä tutkittu., Siksi oletamme, että testosteroni osallistuu maladaptive fibroottisia muutoksia, jotka tapahtuvat seuraavat virtsarakon pistorasiaan tukkeuma.
Materiaalit ja Menetelmät
Hiiren Osittainen Virtsarakon Pistorasiaan Tukkeuma Malli
Kaikki kirurgiset toimenpiteet hyväksyttiin Eläinten Hoidon ja Käytön Komitean Stanley Manne Lasten Tutkimuslaitos. Kahdeksan – kymmenen viikon CD1 uros hiiret (Charles River Labs, Chicago, IL, USA) oli sijoitettu eri häkkeihin välttää muutoksia testosteronin aiheuttama konsernin asunto. Hiiret nukutettiin 3% isofluraanilla ja ne sijoitettiin makuulle., Alavatsaa ajeltiin ja valmistettiin providoni-jodiliuoksella. Nukutuksen tyydyttävän induktion varmistamisen jälkeen tehtiin keskiviivan alavatsan ihon viilto, joka kulkeutui alas vatsan seinämän läpi. Virtsarakon pistorasiaan tukkeuma toteutettiin vuonna muoti samanlainen kuin edellinen kertomus, mutta joitakin eroja (osittainen tukkeuma tai PO-ryhmä) (7). Huomaa, että osittainen tukos on yleensä kutsutaan ”pBOO,” kuitenkin, me katso leikkaus ja kokeellinen ryhmä kuin PO., Kanssa ylöspäin veto virtsarakon, tylppä leikkelyn ympäri virtsarakon kaulan (proksimaalinen eturauhasen uroshiirillä) tehtiin, kun joskus mittaamisesta virtsarakon caudally varmistaa leikkelyn olla anteriorinen ureters. 7-0 polypropeeni ommel oli silloin kulunut noin virtsarakon kaulan ja sidottu alas yli 23 gaugen neulan viereen virtsaputken. Tämän jälkeen neula poistettiin., Jos mies eläimet olivat kastroitu (kastroida osittainen tukkeuma tai CPO), samanaikaisesti kivekset olivat tuoneet pois vatsan viilto, spermatic johdot liitettiin kanssa 6-0 polypropeeni ompeleita ja jyrkästi jakautuneet. Tämän jälkeen vatsan seinä ja iho suljettiin erikseen 5-0 polyglaktiinisaumauksella keskeytyneesti. Sham-eläimille tehtiin sama toimenpide rakkomobilisaatioon asti. Eläinten annettiin toipua, edellyttäen että karprofeeni liuotettiin juomaveteen ja uhrattiin 1 tai 4 viikon kuluttua jäljempänä kuvatuista toiminnallisista tutkimuksista., Seuraava uhraus, jonka kaularangan sijoiltaan alle isofluraani anestesian, eläimet punnittiin ja rakot olivat dissektoitujen tasolla jäljet. Jokainen rakko tyhjennettiin virtsasta ja punnittiin sitten erikseen 12 Shamin, 17 PO: n, 11 CPO: n ja 11 cpot: n hiirillä.
Testosteroni Hallinto
Testosteroni cypionate oli annettu kastroida, osittain tukossa ryhmä klo kastraatio ja viikoittain leikkauksen jälkeen, kun annos oli 10 mg/kg (kastroida osittainen tukkeuma testosteronin tai CPOT-ryhmä)., Hiirille annettu testosteronikorvaushoitoa, verta oli piirretty samaan aikaan uhri ja lähetetään kaupallisiin testosteronin määritys varmistaa, että he saivat riittävää korvaamista (Antech Diagnostiikka, Irvine, CA, USA).
Virtsaamisen Tahra Paperilla (VSOP)
VSOP suoritettiin aamuisin jälkeisen päivinä 1, 7 ja 28 kullekin hiiri. Hiiriä säilytettiin metaboliahäkeissä, joiden pohjana oli Whatman-suodatinpaperi 2 tunnin ajan, ja niille annettiin rajoittamaton pääsy ruokaan ja veteen. Suodatinpaperilevyt imagoitiin., Numero ja kuvio kolot oli huomattava, ja alueen jokaisen virtsaamisen tahra mitattiin käyttäen ImageJ (National Institutes of Health, Bethesda, MD, USA). Tavallisella käyrä luotu virtsaamisen tahrat tunnettu määriä virtsaa, tahra-alue muutettiin mitätön määrä. Max tyhjensi äänenvoimakkuutta analysoitiin.
Histologinen Analyysi
Rakot olivat kiinteä 10% (w/v) formaliinia (Sigma) 24 s, upotettu parafiiniin ja leikataan poikittain kanssa virtsarakon kaulan suuntautunut alas tuottaa 4 µm kohdat. Massonin trikromilla värjättiin osia 4 sham -, 4 PO -, 4 CPO-ja 4 cpot-hiirestä., Osat olivat kuvaamisen 10× ja 40× suurennus käyttäen Leica pystymikroskooppi on yhdistetty kameraan, ja kuvaa oli digitaalisesti tallennettu käyttäen OpenLab for Mac. Col / SM-suhde kvantifioitiin Adobe Photoshopilla aiemmin kuvatulla tavalla ja keskimäärin neljästä 40× osiosta rakkoa kohden. Immunostressoinnissa rakkoja vahvistettiin 4%: ssa (w/v) paraformaldehydistä (em Sciences) valmistettua formaldehydiä yhdessä yössä. Kudoksen pestiin DPBS ja tasapainotettu peräkkäin 20% (w/v) ja 30% (w/v) sakkaroosi (Sigma) vuonna DPBS., Kudokset jäädytettiin kuorimattomiin muotteihin, jotka sisälsivät OCT: ta (Tissue Tech) kuivajää-isopentaanikylvyssä (Sigma).
Immunofluoresenssi-Vasta-aineet
Kiinteä rakot 3 huijausta, 3 PO, 3 CPO, ja 3 CPOT hiiret olivat käytössä. 10 µm: n pätkiä leikattiin kaikkia kokeita varten. Osat pestiin kaksi kertaa PBS: llä, inkuboitiin 5 min huoneenlämmössä PBS + 0.1% Tween (PBT), ja tukossa 30 min huoneenlämmössä 10% aasin seerumia PBT., Sileän lihaksen myosiinin (SMM) oli havaittu samalla tavalla käyttäen rabbit anti-sileän lihaksen myosiinin (Biolääketieteen Teknologioiden, 1:100) yhdessä Alexa Fluor 546 donkey anti-rabbit sekundaarinen vasta-aine (Life Technologies, 1:400).
Tilastoanalyysia
ryhmiä verrattiin anovalla post hoc Student–Newman–Keuls-analyysiin. Tuloksia, joissa P < 0, 05, pidettiin merkittävinä. SPSS v22. 0 hyödynnettiin tilastoanalyysissä. Lukujen virhetangot heijastavat SEM: ää.,
Tulokset
PO Johtaa Toiminnallisia Muutoksia Määräytyy Urodynaamiset Tutkimukset ja Virtsaamisen Tahra Paperilla
Osittainen virtsarakon pistorasiaan tukkeuma tehtiin uros-CD-1 hiirillä ja verrattuna kaksi ryhmää: uros hiiret, joille huijausta leikkaus ja uros hiiriä, joille tehtiin osittainen virtsarakon pistorasiaan tukkeuma kastraatio. Mittasimme kastroiduilla hiirillä seerumin testosteronitasoja ja havaitsimme, että pitoisuudet laskivat (<20 pg/dL) 24 tunnin kuluessa orkiektomian jälkeen., Tukoksen vaikutukset virtsarakon toimintaan määritettiin käyttämällä urodynaamisia tutkimuksia näissä kolmessa ryhmässä. Kuva 1A osoittaa kohonnut huippu virtsaamisen paineet 1 viikko post-tukkeuma PO ja CPO hiirillä verrattuna sham leikkaus hiiriä. Edustavat urodynaamiset merkkiaineet osoittavat myös epävakautta 1 viikon kuluttua PO-ja CPO-hiirillä (Kuva 1c). VSOP suorittaa 1 viikon jälkeen tukos heijastavat vaikutus tukkeuma PO ja CPO hiiriä, jotka ei ole nähneet huijausta leikkaus hiiret (Kuvat 1B,D)., Näin ollen MALLILLAMME PO: lla oli merkittäviä toiminnallisia vaikutuksia virtsaamiseen sekä PO-että CPO-hiirillä 1 viikkoa leikkauksen jälkeen.
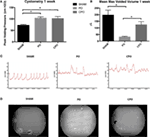
Kuva 1. Kystometria (A) ja keskimääräinen suurin mitattu tilavuus (B) hiiriltä 1 viikon kuluttua hoidon aloittamisesta. Sarakkeet ovat (vasemmalta oikealle) Sham, PO, CPO. C) edustavat jäljitykset kystometrian analyysistä. (D) Edustaja kuvia virtsaamisen tahroja Whatman Paperi asetetaan hiiret 2 h näkyviksi ultra violet imaging. Virhetangot ovat SEM., Tilastollinen merkitsevyys (P < 0.05) on merkitty edellä baareja tähdellä.
Vaikka tukkeuma CPO hiirillä on osoitettu at-1 viikko, vaikutusten estäminen ratkaistiin 4 viikkoa. VSOP tehty 4 viikkoa post-tukos osoittaa, että PO hiiret ovat pysyviä obstruktiivinen virtsaamisen kuvioita pienempiä enintään mitätöidään määriä kuin RAA hiiriä. Samaan aikaan CPO-hiiret saavat takaisin suurimmat mitätöidyt määrät, jotka muistuttavat sham surgery-hiiriä (kuvat 3a–C)., Yleinen kuvio VSOP ja CPO hiirillä on palautunut normaaliksi, kun PO hiiret edelleen osoitettava tahditon ruiskutus virtsan osoittaa menetys virtsarakon ohjaus.
Virtsarakon Remontin jälkeen PO On muuttaa Kastraation
– Olemme huomanneet, että vaikutukset rakon toiminta korreloivat makroskooppinen muutoksia hiiri rakko PO ja CPO hiiriä. Tuolloin hiiri uhrata 4 viikon kuluessa PO, sham rakkoja ilmestyi normaali koko, mutta PO ja CPO virtsarakon olivat selvästi suurentuneet (Kuvat 2A,C–E)., Seuraavat leikkelyn virtsarakon distaalinen virtsarakon kaulan, sitominen, rakot olivat ilmaisseet virtsan ja punnitaan. PO-hiirillä havaittiin rakkopainon lisääntymistä verrattuna sekä sham-leikkaukseen että CPO-hiiriin. CPO-hiirillä ei havaittu lisääntynyttä painoa verrattuna sham-leikkaushiiriin (Kuva 2b). Näiden hiirten rakkojen histologinen arviointi suoritettiin H&e värjäystä ja virtsarakon aluetta, kehää ja paksuutta verrattiin., Sekä CPO ja PO hiirillä osoitti lisääntynyt alue ja ympärysmitta verrattuna sham leikkaus hiirillä, mikä muuttuu kohonnut virtsarakon paineet seuraavat PO (Luvut 2 F,H). Virtsarakon paksuuden lisääntymistä havaittiin kuitenkin vain PO-hiirillä (Kuva 2G). Tämä korreloi alhaisempi virtsarakon painot CPO hiirillä, mikä viittaa siihen, että kasvu virtsarakon koko on lähinnä ”venyttely” virtsarakon lihasten vastakohtana true virtsarakon lihasten liikakasvu tai liikakasvu.
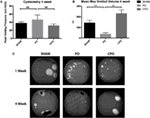
Kuva 3., Cystometry (A) ja max mitattujen tilavuuksien keskiarvo (B) 4 viikkoa Shamin Tai PO: n jälkeen. C) edustavia kuvia Sham -, PO-tai CPO-hiirten tahrien poistamisesta 1 ja 4 viikon kuluttua leikkauksesta. Virhetangot ovat SEM. Tilastollinen merkitsevyys on ilmoitettu edellä baareja tähdellä (**P < 0.01). NS osoittaa, että ero ei ollut tilastollisesti merkitsevä.,
Virtsarakon Fibroosia Lisää seuraavat Osittainen Virtsarakon Pistorasiaan Tukkeuma
voidaan tutkia, jos lisääntyminen virtsarakon massa ja virtsarakon seinämän paksuus johtui yksinomaan lihasten hypertrofia/hyperplasia tai jos osa fibroosia oli mukana, histologinen tutkiminen huijausta, PO, ja CPO hiiri rakot tehtiin 4 viikon jälkeen tukos. Tämä tehtiin käyttämällä sekä Massonitrikromivärjäystä että fibroosin merkkikohtaista immunofluoresenssia (Kuva 4)., Kuten odotettiin, tukoksen jälkeen PO-hiirillä rakkojen havaittiin lisänneen Col / SM-suhdetta. Kastraation myötä kohonnutta Col / SM-suhdetta ei enää havaittu (Kuva 4B). Vaikka luminaalinen virtsarakon tilavuus suureni CPO-hiirillä, lihaskerros ei osoittanut hypertrofiaa, mistä osoituksena oli sama virtsarakon seinämän paksuus kuin sham surgery-hiirillä. Lisäksi arviointi fibroosi erityisiä markkereita Vimentin, Col1a1, ja FSP-1 immunofluoresenssilla osoitti lisääntynyt ilmaisun PO hiirillä verrattuna sham-hiiriä, ja vastaava lasku ilmaisun CPO hiiriä., Näyttää siltä, että kastraation luo edellytykset ei-fibroottiset virtsarakon remontin tapahtuu, väittäen mahdollinen rooli testosteroni erityisesti sovittelijana fibroottiset vastaus virtsarakon vahinkoa.
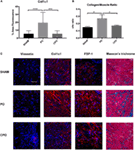
Kuva 4. Fibroottisten proteiinien esiintyminen virtsarakon seinämässä PO: n jälkeen. (A) pylväsdiagrammi, jossa näkyy keskimääräinen pinta-alan fluoresenssi Col1a1: lle. Merkitystä on merkitty * – **P < 0.001 tai ****P < 0.0001. (B) Bar kaavio, jossa Col/SM suhde Sham, PO, ja CPO rakkoja., Merkitsevyyden ilmaisee * P < 0, 05. (C) Edustaja immunofluoresenssi kuvia Vimentin, Col1a1, FSP-1, ja Masson on trichrome. Vasta-ainetahra on punainen ja DAPI-vastatahra sininen. Paneelirivit ovat osioita (ylhäältä alas) Sham, PO, ja CPO. Rivit on merkitty vasemmalle. Suurennuspalkki vasemmassa ylimmässä paneelissa on 100 µm ja se edustaa suurennusta kaikille paneeleille.,
Käyttöönotto Eksogeeninen Testosteroni Kääntää Myönteisiä Vaikutuksia Kastraation jälkeen Osittainen Virtsarakon Pistorasiaan Tukkeuma
– Olemme osoittaneet, että kastraatio, jossa PO on vaimentaa post-obstruktiivinen remontin osalta virtsarakon hypertrofiaa/hyperplasiaa ja fibroosia. Osoittamaan, että tämä on testosteroni-vastauksen jälkeen kastraation, kohortti hiirille tehtiin PO ja testosteroni lisäravinteen. Täällä käytimme joko testosteronia tai sen alennettua tuotetta dihydrotestosteronia (DHT)., DHT on 10-kertainen affiniteetti androgeenireseptorin verrattuna testosteroni ja voi olla maustettu estrogeenin, vähentää todennäköisyyttä, että ne muutokset, joita tapahtuu alkaen testosteroni lisäravinteen on tarkoitus lisätä estrogeenitaso. Max mitätöidään volyymit määritettynä VSOP olivat huomattavasti alhaisemmat CPO plus testosteroni (CPOT) tai CPO plus DHT (CPOD) hiirillä verrattuna CPO hiiret (Kuva 5A). PO-hiirillä (mutta ei CPO-hiirillä) havaitut makroskooppiset ja mikroskooppiset muutokset ilmaantuivat uudelleen CPOT-ja CPOD-rakkoissa., Virtsarakon paino nousi merkitsevästi CPOT-ja CPOD-hiirillä verrattuna CPO-hiiriin (Kuva 5B). Myös cpot-ja CPOD-rakkojen Col/SM-suhdeluvut olivat kasvaneet verrattuna CPO: han (Kuva 5D). Fibroosi merkit olivat myös lisääntynyt CPOT ja CPOD verrattuna CPO rakot kuin oli reaktio Masson on trichrome tahra (Kuvat 5C,E). Nämä löydökset osoittavat, että testosteronin eksogeeninen korvaaminen kuohituilla uroshiirillä palautti täysin virtsarakon tukkeutumisen patologiset vaikutukset., Yhteenvetona kastraation ja testosteronikorvauksen vaikutukset tukevat voimakkaasti miehen androgeenin roolia virtsarakon tukkeutumisen patogeneesissä.
Keskustelua
Pojat syntynyt PUV tehdään kirurginen resektio obstruktiivinen esitteitä pian synnytyksen jälkeen. Huolimatta lievittää virtsarakon pistorasiaan tukkeuma nämä lapset, monet potilaat, joilla PUV edetä virtsarakon heikkeneminen edellyttää ajoittainen puhdas katetrointi riittävästi tyhjentää rakko (3). Nämä muutokset nähtiin usein murrosiän jälkeen., Kliiniset muutokset potilailla, joilla on leikattu venttiilit olivat aiemmin johtuu fysiologisia muutoksia, jotka liittyvät aikuistumiseen, kuten lisääntynyt virtsan suodatus ja hormonaaliset muutokset (1, 5, 9). Havaintomme viittaavat kuitenkin siihen, että androgeenilla voi olla tärkeämpi rooli kuin aiemmin on arveltu. Havaitsemme, että androgeenin läsnäolo tai puuttuminen vaikuttaa erityisesti tukkeuman jälkeen tapahtuviin solumuutoksiin, erityisesti fibroosiin.,
tiedot tutkimuksista, joissa testosteronia täydennettiin potilailla, joilla oli alempien virtsateiden sairaus, saattavat antaa käsityksen androgeenin vaikutuksista virtsarakon sairauteen. Nämä tiedot ovat suhteellisen harva, tulossa pääosin retrospektiivinen tai prospektiivinen havainnoivat tutkimukset ja tutkimukset, joissa testosteroni annettiin hypogonadal tai eugonadal miehet. Kuitenkin nämä tutkimukset viittaavat siihen, että testosteronilisä ei pahenna LUTS (10, 11)., Erityisesti, useita tutkimukset ovat osoittaneet parannusta IPSS pisteet miehet saavat androgeenien ravintolisistä, vaikka monet näistä ei erikseen tutkimuksessa miehet, joiden tiedetään virtsarakon pistorasiaan tukkeuma, vaan kuuluu kohortin käsitelty testosteroni lisäravinteiden ja joilla on eriasteisia LUTS lähtötilanteessa. Yhdessä tutkimuksessa suljettiin pois potilaat, joilla tiedetään olevan virtsarakon kaulan tukos. Koritsiadis ym., teki nimenomaan vertailla oireet ja urodynaamiset parametrit paine-virtaus tutkimukset hypogonadal ja eugonadal miesten ja totesi, seerumin testosteroni taso olla korreloi negatiivisesti rakon paine max virtaus, mutta ei IPSS tai muita urodynaamiset parametrit (12).
testosteronin vaikutusta virtsarakon detrusor-lihakseen on tutkittu myös eläinmalleissa. Tek ja kollegansa totesi, että testosteroni lisäravinteen kirurgisesti kastroitu rotilla johti vähentynyt kollageenin sileän lihaksen suhde ja lisääntynyt cystometric kapasiteetti (13). Shortliffe ym., (14) todettiin, että testosteronia korvaavan kirurgisesti kastroitu rotilla oli myös liittyy lisääntynyt virtsarakon sileän lihaksen sekä lisääntynyt virtsarakon massa (14). Yhdessä nämä tutkimukset osoittavat, että esteetön rotat, testosteroni stimuloi rakon sileän lihaksen kasvun kautta vielä epäselvää mekanismi. Uroskaniineilla tehdyssä iskemia-reperfuusiorakkovammamallissa, Chuang et al. osoitti, että kastraatio suojasi vähentämällä virtsarakon fibroosia ja vähentämällä erilaisten fibroosiin liittyvien merkkiaineiden ilmentymistä (8)., Näiden kastroitujen kanien testosteronilisä johti lisääntyneeseen detrusor-fibroosiin virtsarakon vamman jälkeen. Havaintomme peilaavat näitä löydöksiä ja edustavat ensimmäistä tutkimusta testosteronin vaikutuksesta poikasten hiirten virtsarakon vamman vasteeseen.
samaan aikaan kirjallisuudessa tehtyjen havaintojen vähäisyys sai meidät yllättymään alkuhavainnoistamme. Yksi mahdollinen huolenaihe oli se, että hiiret eivät ole riittävän tukossa ja, että havainnot kastroitu hiiret oli ryhmä, jossa tukos yksinkertaisesti ei tapahdu., Lopulta, me tiedämme, tämä ei ole totta, koska rakot vuonna CPO-ryhmä oli aluksi virtsaamisen tahrat, kuten tukossa ryhmä, oli epänormaali paineita, sillä cystometry, ja oli uusittu rakot. Itse asiassa CPO-hiirten rakot olivat hyvin erilaisia kuin shams, mikä osoittaa, että PO-leikkaus tuotti syvällisiä vaikutuksia. Meidän tulkinta näistä tuloksista on, että tuntia leikkauksen jälkeen, paine kasvaa sisällä virtsarakon seinämän ja, että normaali hiiret, kollageenien ja muut jäykistyminen matriisit on rakennettu estämään rikkoutumista virtsarakon vatsaan., Rakot alkaen CPO hiiret oli hyvin vähän laskeuman kollageenin sisällä tyhjentäjälihaksen lihas, mutta samaan aikaan, tuli erittäin suuri ohuet seinät. On mahdollista, että kun fibroottiset vastaus on heikentynyt korkea paine virtsarakon, se venyy mukautumaan virtsa kertyy. Tämä on tyypillistä, mitä havaitsimme CPO: ssa, mutta ei PO: n ja CPOT: n rakkoja. Niinpä oletamme, että testosteronin rooli voi olla nimenomaan virtsarakon seinämän fibroosin välittäjänä.,
Vaikka työmme nimenomaan hyödynnetään virtsarakon malli määrittää rooli testosteronia lihasten fibroosi vastauksena sileä lihas, uskomme, että tämä tutkimus osoittautuu tärkeää monissa fibroottiset taudin prosesseja, jotka ovat seksi-yhdistys. Tätä ovat tukeneet muutamat kirjallisuustutkimukset. Cho et al. osoitti, että orchiectomy heikensi virtsanjohtimen tukkeutumisen jälkeen todettua munuaisfibroosia. Hiirimallissa, jossa uroshiirillä oli yksipuolinen virtsajohtimen tukos, uroshiirten munuaiset osoittivat alfa-SMA: n ja kollageenin laskeuman lisääntyneen (15)., Samanlainen kuin meidän virtsarakon malli tukos, tämä fibroottiset vastaus oli minimoida, jos samanaikainen orkiektomia suoritettiin virtsanjohtimen tukos. Samanlaisia löydöksiä raportoitiin hiirimallissa, jossa sydämen fibroosi oli seurausta paineen ylikuormituksesta. Tässä vasemman kammion fibroottiset muutokset vaimenivat orkiektomialla. Tähän sisältyi lyhytvaikutteisen TGFß-signalointireitti, jonka tiedetään olevan tärkeää edistää myofibroblast eriyttäminen (16). Ikään liittyvää sydän-ja munuaisfibroosia heikensi myös orchiektomia uroshiirillä (17)., Lisäksi tutkimuksessa Zhu ja työtovereiden, androgeenireseptorin verisuonten sileän lihaksen soluissa oli sekaantunut testosteroni stimuloi sileän lihaksen kalkkiutuminen. Käyttämällä verisuonten sileän lihaksen soluissa, jotka on johdettu sileä lihas-erityisiä androgeenireseptorin tyrmäys hiiri, kalkkeutumista oli pyöristetty vastauksena testosteroni hoito verrattuna villin tyypin sileän lihaksen soluissa (18). Niinpä yhä useammat tutkimukset, myös meidän, löytävät yhteyden testosteronin ja fibroosiin liittyvien patologisten muutosten välillä.,
testosteronin roolin taustalla oleva mekanismi vamman detrusor-vasteen moduloinnissa on edelleen selittämätön. Lisäksi työ tutkii loppupään vaikutukset testosteroni tyhjentäjälihaksen lihas voi paljastaa romaani terapeuttisia tavoitteita, joita voitaisiin hyödyntää estää tai ainakin lieventää haitallisia kudosten remodeling nähnyt asettaminen PO. Lisäksi annos–vaste-tutkimuksia voitaisiin suorittaa määrittää, mitä seerumin testosteroni aiheuttaa haitallisia remontin. Estrogeenin on osoitettu vaimentavan eläinmalleissa kudoshypoksiaa ja siihen liittyvää detrusor-vahinkoa., Lisätutkimukset testosteronin ja estrogeenin välisestä vuorovaikutuksesta detrusorin lihasvasteen moduloinnissa loukkaantumiseen voivat myös auttaa tämän reitin selventämisessä.
Johtopäätös
Nuorten uroshiiriä osittainen virtsarakon pistorasiaan tukkeuma on pienempi korkea paine rakot, jotka ovat fibroottisia. Kastraatioon liittyi suurempia mitattuja määriä, pienempi virtsarakon paino ja vähemmän detrusor-fibroosia. Testosteronin korvaaminen kastraattihiirillä kumosi nämä vaikutukset., Tämä osoittaa, että testosteroni on rooli muuttamalla muutoksia detrusor lihas jälkeen osittainen rakon ulostulotukos hiirillä. Siten, suosittelemme, että lisääntynyt testosteronin pojilla PUV voi edistää vähentynyt virtsarakon toimintaan.
Etiikka-Selvitys
Tämä tutkimus toteutettiin suositusten mukaisesti kirurginen suuntaviivat, Eläinten Hoitoa ja Käyttöä käsittelevä Komitea. Pöytäkirjan hyväksyi Eläinten hoito-ja Käyttökomitea.
tekijätiedot
AF, PF, DB, NK ja GS tiedonkeruu ja-analyysi., AF, PF, RD, ja esim suunnittelu, suunnittelu, ja käsikirjoitus kirjallisesti.
eturistiriita Lausunto
kirjoittajat ilmoittavat, että tutkimus on tehty ilman mitään kaupallisia tai taloudellisia suhteita, jotka voitaisiin tulkita mahdollisia eturistiriitoja.
Rahoitus
Tämä tutkimus tukivat rahoitusta Hartwell Association ESIM.
4. Holmdahl G, Sillen U. Boys posterior virtsaputken venttiilit: tulos koskien munuaisten toimintaa, virtsarakon toiminta ja isyys iässä 31-44 vuotta., J Urol (2005) 174(3):1031–4; discussion 1034. doi:10.1097/01.ju.0000170233.87210.4f
PubMed Abstract | CrossRef Full Text | Google Scholar
5. Holmdahl G, Sillen U, Hanson E, Hermansson G, Hjalmas K. Bladder dysfunction in boys with posterior urethral valves before and after puberty. J Urol (1996) 155(2):694–8. doi:10.1097/00005392-199602000-00094
PubMed Abstract | CrossRef Full Text | Google Scholar
6., Gallo CBM, Miranda AF, Felix-Patricio B, Ramos CF, Cardoso LEM, Costa WS, et al. Effects of castration and hormone replacement in the urinary bladder of rats: structural, ultrastructural, and biochemical analysis. J Androl (2012) 33(4):684–90. doi:10.2164/jandrol.111.014159
PubMed Abstract | CrossRef Full Text | Google Scholar
7. Austin JC, Chacko SK, DiSanto M, Canning DA, Zderic SA., Mies hiiren malli osittainen virtsarakon pistorasiaan tukkeuma paljastaa, muutokset rakon morfologia, supistumista ja myosiini-isoentsyymin ilme. J Urol (2004) 172 (4 Pt 1): 1524-8. doi:10.1097 / 01.ju.0000138045.61378.96
PubMed Abstrakti | CrossRef Koko Teksti | Google Scholar
11. Yassin D-J, El Douaihy Y, Yassin AA, Kashanian J, Shabsigh R, Hammerer PG., Alempien virtsateiden oireita, parantaa testosteronin korvaushoito miesten kanssa viiveellä ilmaantuvia hypogonadismi: 5-vuoden mahdollinen, havaintoihin ja pitkittäinen seurantatutkimus. World J Urol (2014) 32(4):1049-54. doi:10.1007/s00345-013-1187-z
PubMed Abstrakti | CrossRef Koko Teksti | Google Scholar
15. Cho MH, Jung KJ, Jang HS, Kim JI, Park KM. Orchiectomy vaimentaa munuaisfibroosia virtsanjohtimen tukkeutumisen jälkeen vähentämällä oksidatiivista stressiä hiirillä. Am J Nefroli (2012) 35(1):7-16. doi:10.,1159/000334598
PubMed Abstract | CrossRef Full Text | Google Scholar
16. Montalvo C, Villar AV, Merino D, Garcia R, Ares M, Llano M, et al. Androgens contribute to sex differences in myocardial remodeling under pressure overload by a mechanism involving TGF-beta. PLoS One (2012) 7(4):e35635. doi:10.1371/journal.pone.0035635
CrossRef Full Text | Google Scholar
17., Hewitson TD, Zhao C, Wigg B, Lee SW, Simpson ER, Boon WC, et al. Relaksiini ja kastraatio uros hiiret suojaa, mutta testosteroni pahentaa, ikään liittyvä sydämen ja munuaisten fibroosi, kun taas estrogeenit ovat riippumaton tekijä urut size. Endokrinologia (2012) 153(1):188-99. doi:10.1210 / Fi.2011-1311
PubMed Abstrakti | CrossRef Koko Teksti | Google Scholar
18. Zhu D, Hadoke PW, Wu J, Vesey AT, Lerman DA, Dweck MR, et al., Ablation of the androgen receptor from vascular smooth muscle cells demonstrates a role for testosterone in vascular calcification. Sci Rep (2016) 6:24807. doi:10.1038/srep24807
PubMed Abstract | CrossRef Full Text | Google Scholar
Vastaa