PHOTOBIOLOGY az EMBERI LENCSE
Joan E. Roberts
Fordham University, Department of Natural Sciences
113 Nyugat 60th Street, New York, NY 10023
Bevezető
Az elsődleges funkciója az emberi lencse fókusz fény torzítatlan rá a retina. Míg a szem legtöbb összetevőjének átviteli tulajdonságai stabilak, a lencse átviteli tulajdonságai az egész életen át változnak, az 1.ábrán látható módon.,
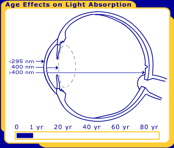
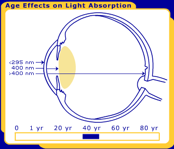
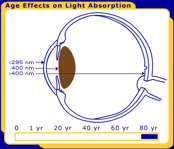
1.ábra. Az emberi lencse változásai az egész életen át. A képen a születés, 40 év, 80 év.
A nap erős fényének való kitettség különös veszélyt jelenthet a szemlencsére, és szürkehályog kialakulásához vezethet , ami rontja a látást., Mind az UV-A, mind az UV-B expozíció a szürkehályog kialakulásának fő kockázati tényezői, különösen a 70 év felettiek esetében,mivel az életkorral a szem képes megvédeni magát a fénykárosodástól. Az UV-sugárzásnak való kitettség a víz, a homok vagy a hó visszaverődéséből különösen káros a szemlencsére .az UV-sugárzás mellett önmagában sok festék, gyógyszer és növényi gyógyszer van, amelyek mind a látható fény, mind az UV-sugárzás jelenlétében szürkehályogot okozhatnak . Ez a fototoxikus reakció nagyon korai szürkehályogot okoz .,
a lencse tisztaságának bármilyen módosítása rontja a retina számára bemutatott kép minőségét, ami nagyban befolyásolja a vizuális érzékelést. Ebben a modulban megismerjük a lencse fotokémiáját és fotobiológiáját, valamint azt, hogy ezek a tulajdonságok hogyan hatnak nemcsak a retinára, hanem az emberi egészségre is .
a szem elülső részének szerkezete(elülső szegmens)
az emberi szem több rekeszből áll, amint az a 2.ábrán látható. A legkülső réteg tartalmazza a sclera – t, amelynek feladata a szemgolyó védelme, valamint a szaruhártya, amely a bejövő fényt a lencsére fókuszálja., E réteg alatt található az íriszet tartalmazó koroid, amelyet uvea néven ismertek. Ez a régió melanocitákat tartalmaz, amelyek pigment melanint tartalmaznak, amelynek feladata a fény szóródásának megakadályozása. Az írisz, a tanuló nyílása kitágul, és összehúzódik a bejövő fény mennyiségének szabályozására. Az írisz és a lencse vizes humorban fürdik. A vizes humor olyan folyadék, amely átlátszó keringési rendszerként szolgál (mi a véráramlás a nem átlátszó szövetekben)., Nem csak fenntartja az intraokuláris nyomást, hanem táplálkozást is biztosít a lencse és a szaruhártya számára, és eltávolítja a szemszövetekből származó törmeléket és hulladékot. A vizes humor nagy koncentrációban tartalmaz különböző antioxidánsokat. A lencse az írisz mögött helyezkedik el. A lencse funkciója az, hogy a fényt torzítatlanul fókuszálja a retinára, amely a szem hátulján van (hátsó szegmens) .

2.ábra. Az emberi szem szerkezete.,
az emberi lencse szerkezete
az emberi lencse szerkezete a 3.ábrán látható. A lencse egy átlátszó szerv, amely a szaruhártya és az írisz mögött helyezkedik el . A lencse külső széle egyetlen hámsejtrétegből áll, valamint egy membránból, amely lefedi az egész szervet . A lencse hámsejtjei nem osztódnak, kivéve, ha javítás alatt állnak. Egyes hámsejtek elveszítik a sejtmagjukat és más organellákat, és lencseszálas sejtekké válnak . Ezek a lencse rostsejtek 30% – os fehérjeoldattal vannak feltöltve, úgynevezett cytosol (oldható) lencsefehérje., Mivel a lencse rostsejtekben kevés a fehérje forgalma, a lencsefehérje károsodása az egész életen át felhalmozódik.

3.ábra. Az emberi lencse szerkezete.
a varrat és az Egyenlítő anatómiai fogalmak a szemészetben. A varrat a lencse varratait jelenti. A varratminták összetettebbé válnak, mivel a lencse külső részéhez több réteg lencseszálat kerül hozzáadásra. Az egyenlítő a lencse legnagyobb részének szélét jelenti (hasonlóan a földgömb egyenlítőjéhez).,
mikor káros a fény az emberi lencsére?
bár a környezeti fény többnyire jóindulatú, számos olyan körülmény létezik, amelyek mellett a környezeti fény kitettsége károssá válik. Annak megállapításához, hogy a fény káros-e, figyelembe kell venni a következő tényezőket: intenzitás, hullámhossz, sérülés helye, oxigénfeszültség, kromofórok, védelmi rendszerek, javítási mechanizmusok.
intenzitás. Minél nagyobb a fény intenzitása, annál valószínűbb, hogy károsítja a szemet. A fény, amely általában nem lehet káros, akut károkat okozhat, ha elég intenzív., Például jól ismert, hogy a szem károsodhat (ideiglenesen vagy véglegesen) a hó (hó vakság) fényvisszaverő napfényének való kitettség, vagy a napfogyatkozás során a napra nézve . Növekszik az UV sugárzás a védő ózonréteg elvékonyodásával . Hasonlóképpen, a szem képes fenntartani az UV-A vagy UV-B kibocsátású mesterséges fényforrások károsodását . A kumulatív fénykárosodás a hosszabb ideig tartó kevésbé intenzív expozícióból ered, és gyakran az életkorral összefüggő védelem elvesztésének eredménye .
, A napból vagy mesterséges fényforrásokból származó környezeti sugárzás változó mennyiségű UV-C (100-280 nm), UV-B (280-315 nm), UV-A (315-400 nm) és látható (400-700 nm) fényt tartalmaz. Minél rövidebb a hullámhossz, annál nagyobb az energia, ezért annál nagyobb a biológiai károsodás lehetősége. Bár a hosszabb hullámhosszak kevésbé energikusak, mélyebben behatolnak a szemébe .
annak érdekében, hogy fotokémiai reakció következzen be, a fényt egy adott szemszövetben fel kell szívni., A főemlős / emberi szem egyedi szűrési jellemzőkkel rendelkezik, amelyek meghatározzák, hogy a szem melyik területén minden fény hullámhossza felszívódik. A 295 nm alatti UV-sugárzást az emberi szaruhártya szűri a lencse eléréséből. Ez azt jelenti, hogy a legrövidebb, legenergikusabb hullámhosszú fény (minden UV-C és néhány UV-B) kiszűrésre kerül, mielőtt elérnék az emberi lencsét. A legtöbb UV-fényt a lencse elnyeli, de a pontos hullámhossz-tartomány az életkorától függ. Felnőtteknél a lencse elnyeli a fennmaradó UV-B-t és az összes UV-A-T (295-400 nm), ezért csak a látható fény jut el a retinába., A nagyon fiatal emberi lencse azonban egy kis UV-B fényt (320 nm) továbbít a retinára, míg az idős lencse kiszűri a rövid kék látható fény nagy részét (400-500 nm). Az átvitel fajonként is különbözik; a főemlősöktől eltérő Emlősök lencséi 295 nm-nél hosszabb UV-sugárzást továbbítanak a retinába .
a lencse Fénykárosodásának helye. A lencse két részből áll, amelyek a leginkább érzékenyek a károsodásra: a (külső) hámsejtekből és a (belső) rostmembránból. A hámsejtek szabályozzák a lencse szállítását., Közvetlen kapcsolatban vannak a vizes humorral, és a leginkább érzékenyek a fototoxikus károsodásokra. Ezeknek a sejteknek a károsodása könnyen veszélyeztetné a lencse életképességét . A rostmembrán fotokémiailag károsodhat a lipidek és/vagy a fő belső membránfehérje károsodása révén .
a fototoxikus reakciók a DNS és bizonyos aminosavak (hisztidin, triptofán, cisztein) módosításához és/vagy a szenzibilizáló cytosol lencsefehérjékhez való kovalens kötődéséhez vezethetnek ., A kovalensen kötött kromoforok ezután endogén szenzibilizátorként működhetnek, és hosszan tartó fényérzékenységet okozhatnak. Ezenkívül a cukorbetegséggel kapcsolatos lencsefehérjék nem fotokémiai indukált módosítása van. A magas glükózkoncentráció a lizinmaradékok epszilon-amino csoportjainak glikozilációjához vezet. Az ilyen típusú károsodások mindegyike megváltoztatja a lencse anyag törésmutatóját, ami aggregációhoz és végső soron opacifikációhoz vezet (szürkehályog) ., A nemrégiben kifejlesztett technika (ScanTox) a lencse optikai minőségének (fókuszálásának) nagyon korai változásait méri, még akkor is, ha a sérülés a lencse homályosodását okozza .
Chromophores. A kromofor olyan anyag, amely elnyeli a fényt. A szemkromofor lehet egy endogén vegyület, amely természetesen jelen van a szemben, vagy egy exogén szer, amely átjutott a vér-szem gátakon, és behatolt egy adott helyre. Annak érdekében, hogy a fény károsítsa a lencsét, a fényt először a lencse egyes rekeszében található kromofórnak kell felszívnia.,
A) endogén (természetesen előforduló) kromoforok az emberi lencsében. Az emberi lencse kromofórjai az egész életen át változnak, amint az a 4a. és b. ábrán látható.az emberi szemnek valójában kevés károsodása van a fénytől a középkor előtt. Ennek oka az, hogy a felnőtt emberi lencse sárga kromofórokat (3-hidroxi-kurenineket) tartalmaz, amelyek elnyelik a fényt, de felszabadítják az energiát, mielőtt esélye lenne bármilyen károsodásra ., Tehát a felnőtt emberi lencsében jelen lévő kynurenin kromoforok nemcsak biztonságosak, hanem UV-sugárzás szűrésével védik a retinát, ezáltal megakadályozzák a retina elérését és károsodását . Középkor után a növekvő mennyiségben előállított enzim (kynurenin amino transzferáz) a védő kromofórokat (3-OH kynurenin és annak glükózidja) romboló kromofórokká, xanturensavvá és xanturenikus glükóziddá alakítja . Amikor ezek a xanturén vegyületek elnyelik a fényt , reaktív oxigén fajokat (egysínű oxigént és/vagy szuperoxidot) termelnek, amelyek károsítják a lencsefehérjéket ., Egy másik kromofor, az endogén triptofán folyamatos fotooxidációjából képződött n-formil-kynurenin is termel egysejtű oxigént és szuperoxidot, ami károsítja a lencsefehérjéket . Így a xanturénsav és az n-formil-kynurenin valószínűleg az életkorral összefüggő szürkehályog kialakulásáért felelős kromofórok jelöltjei.

4a. Ahogy a lencse öregszik, a kromofórok megváltoztatják az emberi szem színét a tiszta (középső) színről a sárgára (jobb felső sarokban)., Az emberi lencse öregedési változásainak eredményeként a lencse elhomályosulása következik be, amelyet szürkehályognak neveznek (bal felső sarokban). A tehén lencsék (alsó) és más nem főemlősök egész élettartama alatt tiszta lencsékkel rendelkeznek.
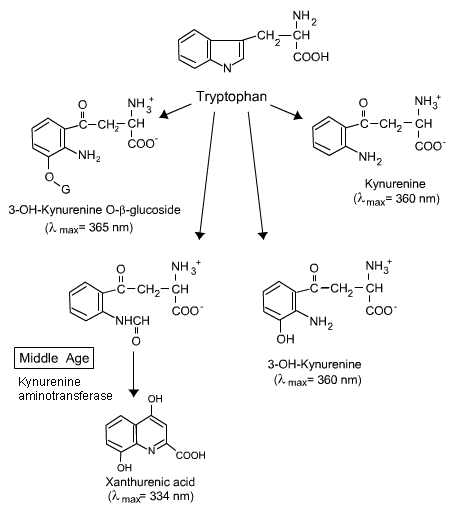
4b. kor. Vegye figyelembe a változást középkorú. További információkért lásd a fenti szöveget.
b) xenobiotikumok vagy exogén kromoforok a lencsében., Intenzív vagy felhalmozódott UV-B vagy UV-A sugárzás közvetlen károkat okoz az emberi lencsében. A fény aktivált (fényérzékenyített) gyógyszer, növényi gyógyszer (Hypericin Orbáncfűben) vagy nanorészecskék jelenlétében azonban a betegeket fokozott szemkárosodás fenyegeti a környezeti UV sugárzás és a látható fény miatt ., Az, hogy egy adott vegyi anyag képes fototoxikus mellékhatásokat előállítani a szemben, számos paramétertől függ, beleértve: 1) a kémiai szerkezetet; 2) a gyógyszer abszorpciós spektruma; 3) a gyógyszer kötődése a szemszövethez; és 4) a vér-szem akadályok átlépésének képessége.
bármely triciklikus, heterociklusos vagy porfirin gyűrűs szerkezetű vegyület potenciális szemkromofor, ha abszorbanciája van a szaruhártya levágása felett (>295 nm). Amikor ezek az exogén (külső) szenzibilizátorok kötődnek a szemszövetekhez (azaz, a lencse retenciós ideje meghosszabbodik, a potenciális veszély pedig fokozódik. Az amfifil vagy lipofil anyagok képesek átlépni a legtöbb lentikuláris akadályt . A lencsét a vizes humor táplálja, és viszonylag nehéz egy anyag számára, hogy lenyeléssel átjusson a vizes humoron a lencsébe. Azonban, ha egyszer a lencsébe kerül, az idegen anyag eltávolítása is nehéz.
oxigén feszültség. A lencse oxigénfeszültsége nagyon alacsony, de elegendő a fotooxidáció kialakulásához .
védelmi rendszerek., A lencse nagyon hatékony védelmi rendszerrel rendelkezik a fény-és sugárzáskárosodás ellen. A lencse antioxidáns enzimeket (szuperoxid-diszmutázt (SOD) és katalázt), valamint antioxidánsokat (E, C, lutein, glutation) tartalmaz, amelyek védik az oxidatív és fotoindukált károsodástól . Sajnos, a legtöbb ilyen antioxidánsok, védő enzimek csökken kezdődő negyven éves , így a lencse védtelen fénykárosodás.
javítás., A perifériás lencse hámsejtjei képesek javítani az UV-B által indukált DNS keresztkötéseket (ciklobután-pirimidin-dimerek és 6-4 pirimidin-pirimidon) , de az UV-A-nak való bármilyen további expozíció zavarja a sejtek javítását. Mivel kevés a lencsefehérjék forgalma, a lencsefehérjék károsodása acumulates .
a lencse Fénykárosodásának mechanizmusa
Fotooxidáció. Az intenzív fény közvetlen DNS-károsodást okozhat, de kevésbé intenzív fény esetén a szem fototoxidációs reakcióval károsodik., A fotooxidációs reakciókban a szem kromofórja elnyeli a fényt és oxidál bizonyos aminosavakat és / vagy nukleinsavakat, ami az egész lencse károsodását eredményezi. A kromofor lehet endogén (természetes) vagy exogén (gyógyszer, gyógynövény vagy Nanorészecske, amely felhalmozódott a szemben). A fény abszorpciója gerjesztett szingulett állapotba gerjeszti a kromofórt, amely ezután keresztezi a rendszert, majd eléri a triplett állapotot., Triplett állapotában a kromofor vagy egy I. típusú (szabad gyök) vagy II .típusú (singlet oxygen) mechanizmuson keresztül jut el az esetleges károsodáshoz. A fotooxidáció a lencsében I-es vagy II-es típusú mechanizmussal, vagy mindkettő egyidejűleg fordulhat elő.
A chromophores a felnőtt emberi lencse lehet izgatott fény, de jönnek le, gerjesztett állapot (trikó) nagyon gyorsan (ns), így nincs esély arra, hogy eléri a triplett állapot, hogy káros aktív intermedierek, ezért okoz kárt a lencse ., Azonban, ha a hatékony fényérzékenyítők, xanturensav, ez glükozid és N-formil kynurenin vannak jelen a lencse és a lencse ki van téve az UV sugárzás, képesek arra, hogy a hármas megfelelő hatékonysággal (kvantum hozam) alkotnak reaktív oxigén fajok és a szabad gyökök, amelyek aztán viszont kár lencse Szövet.
szürkehályog
indukciós mechanizmus. Az emberi lencse általában 40 éves korig átlátszó. Ez az átláthatóság a fehérje rostok rendes elrendezésének eredménye a lencsében ., Középkorú korban a szem természetes enzimatikus és antioxidáns védelme Az UV-A és UV-B ellen elvész, ugyanakkor növekszik a fotokémiailag aktív kromoforok termelése. Mivel a lencse elnyeli a környezeti fényt, ezek a kromofórok fotoaktiváltak, és reaktív oxigén fajokat termelnek, mint például a szingulett oxigén és a szuperoxid. A lencsefehérjék (alfa, béta, gamma kristályok) denaturálódnak, vagy a lencse hámsejtjei már nem képesek javítani a környezeti fény károsodását ., 70 éves korára a lencse végül elég felhős lesz ahhoz, hogy megakadályozza a látást, és az egyénről azt mondják, hogy életkorral összefüggő szürkehályog van (4a ábra) .
szürkehályog is kialakulhat egy sokkal korábbi korban, amikor a személy ki van téve a túlzott UV-sugárzás, cigarettafüst és a légszennyezés, fényérzékenyítő gyógyszert, szteroidok, vagy a cukorbetegség. Ezeknek a szürkehályogoknak a kiváltó oka a lencse hámsejtjeinek és a lencsefehérjéknek oxidatív (és fototoxidatív) károsodása is.,
a szerkezeti integritás fenntartása különösen fontos a lencsefehérje-alfa-kristály szempontjából, mivel molekuláris chaperonként szerepet játszik. az alfa-kristály két polipeptidből, az A-ból és a B-ből áll, amelyek kis hősokk fehérjék, amelyek megakadályozzák az UV (A és B) által kiváltott fehérje aggregációt . A lencse hámsejtjeiből származó alfa-kristályos termelés hozzáadásával és eltávolításával Andley kimutatta, hogy az alfa-kristály természetes védelmet nyújt a lencsesejtek UV-sugárzás károsodásával szemben . az alfa-Krisztallin védelmet nyújt a védő (kataláz) enzimaktivitás UV-A gátlásával szemben is ., Az alfa-kristályok károsodásának specifikus helyeit mind endogén, mind exogén kromofórokkal tömegspektrometriával és monoklonális antitest-technikákkal detektálták . A diabéteszes szürkehályogban található fejlett glikációs végtermékek fényérzékenyítőként is viselkedhetnek, és oxidálhatják a lencsefehérjéket .
minden endogén vagy exogén oxidáció denaturálja a lencsefehérjéket, csökkenti azok oldhatóságát, végül pedig a lencse átlátszóságának elvesztését eredményezi, amelyet szürkehályognak neveznek., A lencse központi részében előforduló szürkehályog nukleáris szürkehályogként ismert, a lencse perifériáján előforduló szürkehályog pedig kortikális szürkehályogként ismert. A szürkehályog ritkább formáját hátsó subcapsularis szürkehályognak nevezik. Ezt a szürkehályogot általában genetikailag összekapcsolják, születéskor vagy nagyon korai életkorban, vagy szteroid használat vagy cukorbetegség következtében fordul elő .
diagnózis és kezelés., A szürkehályog könnyen diagnosztizálható “réslámpa” vagy ophthalmoscope használatával, amely a lencsét az átláthatóság hiánya miatt vizsgálja, és meghatározza a homályosodás helyét és sűrűségét. Ezenkívül a látásélesség-teszt meghatározza, hogy a beteg milyen jól látja a szürkehályogot. Ha jelentős látásvesztést észlelnek, a kezelés a lencse műtéti eltávolítása. Ezt a lencsét általában egy UV-A és UV-B szűrőt tartalmazó intraokuláris műanyag lencsével helyettesítik, hogy helyettesítsék a szürkehályog-lencse eltávolításából elveszített fókuszálási és szűrési teljesítményt ., A közelmúltban, az intraocularis mesterséges lencse már rendelkezésre álló rövid kék fény szűrő (400 – 440 nm), amelyek fontos, hogy megvédje az idősek a makula degeneráció a cukorbeteg a diabeteses retinopathia .
megelőzés. Ha megakadályozza a fény izgalmas endogén vagy exogén kromofórok a lencse, vagy blokkolja a kár reaktív oxigén fajok antioxidánsok, megakadályozhatja vagy késlelteti szürkehályog kialakulását .
a) napszemüveg. Mind az UV-A, mind az UV-B nem szükséges sem a látáshoz, sem a cirkadián válasz kiváltásához., Másrészt mind az UV-A, mind az UV-B szürkehályogképződést okoz. Ezeknek a hullámhosszoknak a szemészeti expozícióból történő eltávolítása nagymértékben csökkenti a korai szürkehályog kialakulásának kockázatát. Ez könnyen elvégezhető olyan napszemüveg viselésével, amely blokkolja a 400 nm alatti hullámhosszokat . A szem geometriája miatt azonban ezeknek a szemüvegeknek körbevett napszemüvegeknek kell lenniük, hogy megakadályozzák a fényvisszaverő UV-sugárzás elérését a szem felé.
b) Az antioxidánsok kora óta csökkentik az antioxidánsok normál termelését a lencsében , növelve az étkezési gyümölcsöket és zöldségeket, javasolták a hiányzó védelem pótlását ., Ezenkívül a vitaminokkal és antioxidánsokkal-köztük az E-vitaminnal és a luteinnel-történő kiegészítés különösen hatékonynak bizonyult az életkorral összefüggő szürkehályog visszaszorításában .
a kiegészítőknek kiegyensúlyozottnak kell lenniük, mivel káros oxidációs reakciók fordulhatnak elő, ha csak egy antioxidánst veszünk . A National Eye Institute által szponzorált AREDS-ben (életkorral összefüggő szembetegség-vizsgálat) azt találták, hogy a túlzott béta-karotin összefüggésbe hozható a dohányosok tüdőrákjának fokozott kockázatával, míg a túlzott Zn összefüggésbe hozható a prosztatarák fokozott kockázatával., Mivel a lutein, nem a béta-karotin, a lencse és a retina természetes karotinoidja, a túlzott béta-karotinnal történő kiegészítés nem csak a szem védelmére felesleges, hanem a dohányzókra és a korábbi dohányzókra is veszélyes. Más természetes termékek, mint például a zöld tea, amely polifenolokat (epigallocatechin gallátot) és Ashwagandha (Withania somnifera gyökere) tartalmaz, amelyeket a hagyományos ayurvédikus orvoslásban használnak, szintén kimutatták, hogy késleltetik a fény okozta károsodást a lencsében .
következtetések
a szürkehályog kialakulása korral összefüggő betegség. A legtöbb ember 70 éves korukra szürkehályogot képez., Mind az UV-A, mind az UV-B nagyon fontos kockázati tényezők a korai szürkehályog kialakulásához. Ezen túlmenően, expozíció még látható fény jelenlétében szteroidok, fényérzékenyítő gyógyszerek, kozmetikumok, nanorészecskék drámaian növeli a korai szürkehályog. Az UV-sugárzás elkerülése megfelelő napszemüveggel, valamint az oxidáló és redukáló antioxidánsok megfelelő kombinációja segíthet az idősek ezen vakító zavarának megszüntetésében vagy megszüntetésében.
Andley UP (2008) the lens epithelium: focus on the expression and function of the alpha-crystallin chaperones., Int J Biochem Cell Biol. 40:317-23.
Andley UP (2007) Crystallins in the eye: Function and pathology. Prog Retin Eye Res. 26: 78-98.
Andley U P, Rhim JS, Chylack Jr LT, Fleming TP (1994) Propagation and immortalization of human lens epithelialis cells, Invest. Ophthalmol. Vis. Sci., 35:3094-3102.
Andley UP, Patel HC, Xi JH, Bai F (2004) Az UV-a sugárzásra érzékeny gének azonosítása az emberi lencse hámsejtjeiben cDNA mikroarrays segítségével. Fotochem. Fotobiol. 80, 61-71.,
Andley UP, Song Z, Mitchell DL (1999) DNA repair and survival in human lens epithelialis cells with extended élettartam. Curr Eye Res. 18:224-30.
Argirov OK, Lin B, Ortwerth BJ (2004) 2-ammonion-6- (3-oxidopiridinium-1-Il) hexanoát (OP-lizin) egy újonnan azonosított fejlett glikációs végtermék szürkehályog és idős emberi lencsékben. J. Biol. Chem. 279:6487-6495.
Argirova MD, Breipohl W (2002) a glikált fehérjék fokozhatják a fotooxidatív stresszt idős és diabéteszes lencsékben. Szabad Radic. Res.36:1251-1259.,
Ayala MN, Michael R, Soderberg PG (2000) hatása expozíciós idő UV sugárzás által kiváltott szürkehályog Invest Ophthalmol Vis Sci. 41: 3539-43. Bachem, A. (1956) Ophthalmic action spectra. Am. J. Ophthalmol. 41: 969-975.
Balasubramanian D (2000) ultraibolya sugárzás és szürkehályog. J. Szemészeti Farmakol. Therap. 16, 285-297.
Balasubramanian D (2005) Photodynamics of Cataract: an Update on endogén Chromophores and Antioxidants. Fotochem. Fotobiol. 81:498-501.
Benedek GB (1971) Theory of transparency of the eye. Appl. Optika 10:459-473.,
Bohow TW, West SK, Azar A, Munoz B, Sommer A, Taylor H R(1989) Ultraviolet light exposure and risk of posterior subcapsular cataractsArch. Szemészet 107: 369-372.
Barker, FM, Brainard GC és Dayhaw-Barker P (1991). Befektetni. Ophthalmol. Vis. Sci. 32. p., 1083.
Bassnett S and Mataic D (1997) kromatin degradáció a J. Cell Biol szemlencse Rostsejtjeinek Differenciálásában. 137: 37-49.,
Busch M, Gorgels TG, Roberts JE, van Norren D (1999) az N-acetilcisztein két sztereoizomerjének hatása az UVA és a kék fény fotokémiai károsodására a patkány retinájában. Fotochem. Fotobiol. 70:353-358.
Coroneo MT (1990) Albedo koncentráció az elülső szemben: olyan jelenség, amely bizonyos Napbetegségeket talál. Szemészeti. Szurgut 21: 6066.
Dillon J and Atherton SJ (1990) Time Resolved Spectroscopic Studies on the intakt Human Lens. Fotochem. Fotobiol. 51 :465-468.
Dillon J (199) a szem Fotofizikája és Fotobiológiája. J. Photochem.Fotobiol. B. Biii. 10:23-40.,
Dovrat A, Sivak JG (2005) hosszú távú lencse szervkultúra rendszer a lencse optikai minőségének ellenőrzésére szolgáló módszerrel. Photochem Photobiol. 81:502-505.
Edge R, a Föld EJ, McGarvey DJ, Mulroy L, Truscott TG (1998) Relatív egy-elektron-csökkentési potenciálok a karotinoid radikális kationok, valamint az egyes karotinoidok az E-vitamin radikális kation. J. Am. Chem. Soc. 120:4087-4090.
Edge R, McGarvey DJ, Truscott TG (1997) a karotinoidok, mint antioxidánsok-a felülvizsgálat. J. Photochem. Fotobiol. B: Biol. 41:189-200.
Falkner-Radler CI, Benesch T,Binder S., (2008) kék fényszűrő intraokuláris lencsék vitrectomiában szürkehályog műtéttel kombinálva: randomizált, kontrollált klinikai eredmények trial.Am J Ophthalmol. 145:499-503.
Finley EL, Dillon J, Crouch RK, Schey KL (1998). A triptofán termékek azonosítása oxidációs szarvasmarha-Alfa-kristályban. Protein Sci., 7:2391-2397.
Finley EL, Dillon J, Crouch RK, Schey KL (1998) a szarvasmarha-alfa-kristályok radiolízis által kiváltott oxidációja. Fotochem. Fotobiol. 68:9-15.
Finley EL, Busman M, Dillon J, Crouch RK, Schey KL (1997) photooxidation sites in bovine alpha-crystallin., Fotochem. Fotobiol. 66:635-641.
Giblin FJ (2000) glutation: a Vital Lens antioxidáns. J. Ocul. Farmakol. Her. 16: 121-135.
Horwitz J, Zigman S (1997) az alfa-kristályok védik a katalázt az UV-károsodás ellen? Biol Bull. 193:254-255.
Jacques PF, Chylack LT Jr, Hankinson SE, Khu PM, Rogers G, Friend J, Tung W, Wolfe JK, Padhye N, Willett WC, Taylor A. (2001) hosszú távú tápanyagbevitel és korai életkorral összefüggő nukleáris lencse opacities. Arch Oftalmol. 119:1009-1019.,
Khachik F, Bernstein PS, Garland DL (1997) lutein és zeaxantin oxidációs termékek azonosítása emberi és majom retinákban. Befektetni. Ophthalmol. Vis. Sci. 1802-1811.
Krisna CM, Uppuluri S, Riesz P, Zigler Jr JS, Balasubramanian D (1991) A Study of the Photodynamic Efficiencies of Some Eye Lens Constitutions. Fotochem. Fotobiol. 54:51-58.
Kuszak JR, Peterson KL, Sivak JG, Herbert KL. (1994) a lencse anatómiájának és az optikai minőségnek a kölcsönhatása. II. főemlős lencsék. Exp Eye Res.59:521-35.,
Kwan M, Niinikoske J, Hunt TK (1971). Befektetni. Ophthalmol. 11:108-111.
Lyle BJ, Mares-Perlman JA, Klein BE, Klein R, Greger JL (1999) antioxidáns bevitel és az életkorral összefüggő nukleáris szürkehályog kockázata a Beaver Dam Eye vizsgálatban. Am. J. Epidemiol. 149:801-809.
Malina HZ, Martin XD (1996) Xanturensav-származék képződés a lencse felelős szenilis szürkehályog emberben. Graefes Arch. Clin. Felh.Ophth., 234: 723-730
McLaren JW, Dinslage S, Dillon JP, Roberts JE, Brubaker RF (1999) Befektetni. Ophthalmol. Vis. Sci. 39:1899-1909.
Merriam JC (1996) a fény koncentrációja az emberi lencsében. Trans.Am. Ophthalmol. Soc. 94: 803-918.
Norval M,Cullen AP, de Gruijl FR, Longstreth J, Takizawa Y, Lucas RM, Noonan FP, van der Leun JC. (2007). A sztratoszféra ózonrétegének kimerüléséből és az éghajlatváltozással való kölcsönhatásából eredő emberi egészségre gyakorolt hatások. Photochem Photobiol Sci. 6:232-51.,
Olmedilla B, Granado, F, Blanco I, Vaquero M (2003) Lutein, de nem alfa-tokoferol, a kiegészítés javítja a vizuális funkciót az életkorral összefüggő szürkehályogban szenvedő betegeknél: egy 2 éves kettős vak, placebo-kontrollos kísérleti vizsgálat. Tápé 19., 21-24.
Roberts JE (2008)” Drug Induced Ocular Phototoxicity “In: Marzulli and Maibach’ s Dermatotoxicology, 7th Edition, edited by H. Zhai, K-P Wilhelm, and H. Maibach, Chapter 28, pp 269-278. Taylor & Francis Group, Boca Raton, Florida.
Roberts JE, Wielgus AR, Boyes WK, Andley U, Chignell CF., (2008) Phototoxicity and cytotoxicity of fullerol in human lens epithelial cells. Toxicology and Applied Pharm 228:49-58.
Roberts JE (2002) Screening for Ocular Phototoxicity. International Journal of Toxicology 21:491-500.
Roberts JE, Finley EL, Patat SA, Schey K L (2001) Photooxidation of Lens Proteins with Xanthurenic Acid: A Putative Chromophore for Cataractogenesis. Photochem. Photobiol. 74: 740-744.
Roberts JE. (2001) Ocular phototoxicity. J. Photochem. Photobiol. B: Biology 64, 136-143.,
Roberts JE, Wishart JF, Martinez l Chignell CF (2000) Xanturensavval végzett fotokémiai vizsgálatok. Fotochem. Fotobiol. 72: 467471.
Roberts JE (2000) Light and Immunomodulation. NY Acad Sci. 917:435-445.
Roberts JE, Roy D, Dillon J (1985) a borjúlencse fő intrinsic protein (MP26) fényérzékenyített oxidációja hematoporfirinnel. Curr. Eye res. 4: l8l-185.
Rodriguez-Galietero A, Montes-Mico R, Munoz G, Albarran-Diego C. (2005) Blue-light filtering intraocular lens in Diabetes: contrast sensitivity and chromatic discrimination. J Szürkehályog Refract Surg., 31:2088-2092.
Samiec PS, Drews-Botsch C, Flagge EW, Kurtz JC, Sternberg P, Reed RL Jones DP (1998) glutation in human plasma declines in association with aging, age-related macular degeneration and diabetes. Szabad Radic. Biol. Med. 24:699-704.
Schalch W and Chylack LT Jr, (2003) antioxidáns mikrotápanyagok és szürkehályog. az AREDS és REACT cataract vizsgálatok áttekintése és összehasonlítása. Ophthalmologe 100, 181-189.
Schey KL, Little M, Fowler JG, Crouch RK (2000) jellemzése emberi lencse fő intrinsic fehérje szerkezet, befektetni. Ophthal. Vis Sci., 41 175-182.,
Schey KL, Patat S, Chignell CF, Datillo M, Wang RH, Roberts JE (2000) a lencsefehérjék fotooxidációja hypericinnel (a Szent János sörce hatóanyaga). Fotochem. Fotobiol. 72:200-207.
Seth RK, Kharb S (1999) az alfa-tokoferol védő funkciója az emberek Szürkehályogogenezisének folyamata ellen. Ann. Nutr. Metab. 43: 286-289.
Sliney DH (2007) Comment : Spectral transmission of IOLs expressed as a virtual age. BRJ. 91:1261-1262.
Sliney DH (2005) expozíciós geometria és spektrális környezet határozza meg az emberi szemre gyakorolt fotobiológiai hatásokat. Photochem Photobiol., 81:483-489.
Sliney, D. H. (1997) az orvosi fényforrások optikai sugárzásbiztonsága. Phys. Med. Biol. 42:981-996.
egyenes R, tüskék JD (1985) a biomolekulák Fényérzékenyített oxidációja. In: O. Singlet, Editor, A. A. Frimer, Editor, Polymers and Biopolimers Vol. IV, CRC Press, Boca Raton, FL, 91-143.
Staniszewska MM, Nagaraj RH. (2005) a humán lencsefehérjék 3-hidroxi-kinurenin által közvetített módosítása: egy jelentős módosítás struktúrájának meghatározása monoklonális antitest alkalmazásával. J Biol Chem. 280:22154-64.,
Thiagarajan G, Venu T, Balasubramanian D (2003) megközelítések a szürkehályog vakságának természetes antioxidánsokon keresztül történő enyhítésére: Ashwagandha (Withania somnifera) használata. Curr. Sci. 85, 1065-1071.
Thiagarajan G, Shirao E, Ando K, Inoue A, Balasubramanian D (2002) szerepe xanthurenic acid 8-o-béta-glükozid, egy új fluorofor, amely felhalmozódik a brunescent emberi szemlencsében. Fotochem. Fotobiol. 76, 368-372.
van Norren D, van De Kraats J. (2007) az intraokuláris lencsék spektrális átvitele virtuális korban kifejezve. Br J Szemészeti; 91: 1374-1375.,
Yeum KJ, Shang FM, Schalch WM, Russell RM, Taylor a (1999) zsírban oldódó tápanyagkoncentráció az emberi szürkehályog lencse különböző rétegeiben. Curr.Eye Res. 19: 502-505.
Zigman S, McDaniel T, Schultz J, Reddan J (2000) az intermittáló UVA expozíció hatása a tenyésztett lencse hámsejtjeire. Curr Eye Res. 20: 95-100.
Zigman S, Rafferty NS, Rafferty KA, Lewis N (1999) A zöld tea polifenoljainak hatása a lencse fotooxidatív stresszére. Biol-Bull. 197: 285-286.
Zigman S (2000) Lens UVA photobiology. J Ocul Pharmacol Ther. 16:161-165.
Vélemény, hozzászólás?