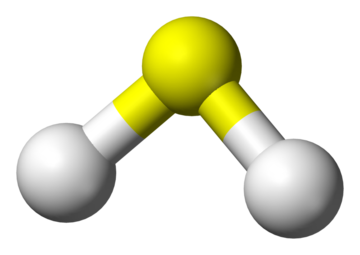
figuur 1. Een bal en stok model van waterstofsulfide. De witte ballen zijn waterstof en de gele bal is zwavel.
waterstofsulfide is een chemische stof met de formule H2S. waterstofsulfide is een gevaarlijk, kleurloos gas dat van nature voorkomt in veel aardolieproducten. In het bijzonder, het maakt vaak aanzienlijke hoeveelheden ruw aardgas. Het heeft een duidelijke “rotte ei” geur bij lage concentraties., Langdurige blootstelling zal resulteren in olfactorische vermoeidheid, dat is het verlies van het vermogen om het te ruiken. Bij hoge concentraties waterstofsulfide gaat het vermogen om het te ruiken onmiddellijk verloren. Waterstofsulfide is niet alleen schadelijk voor de menselijke gezondheid als verstikkend middel, maar is ook ontvlambaar en explosief.
waterstofsulfide komt voor in natuurlijke afzettingen of kan door menselijke activiteiten worden geproduceerd. Waterstofsulfide komt bijvoorbeeld van nature voor in ruwe olie, aardgas en in warmwaterbronnen. Bacteriële afbraak van menselijk en dierlijk afval produceerde ook waterstofsulfide., Mensen geven waterstofsulfide vrij door petroleumboringen en raffinage, afvalwaterzuivering en papierfabrieken.
enkele aanvullende eigenschappen van waterstofsulfide zijn in onderstaande tabel weergegeven.
| chemische formule | H2S | Molaire massa | 34.,0809 gram/mol | smeltpunt | -82oC | kookpunt | -60oC |
het waterstofsulfidegehalte van aardgas is een van de belangrijkste veiligheidsrisico ‘ s van aardgas.het gebruik van aardgas. Aardgas met bijzonder hoge niveaus van waterstofsulfide wordt aangeduid als zuur gas. Sommige van deze zwavel kan worden verwijderd door middel van een “verzoeting” proces, genaamd het “amine proces” of meer in het algemeen het “Girdler proces”., Het wordt gebruikt in de meeste gas zoeting operaties en wordt voornamelijk gedaan met behulp van amine oplossingen die het waterstofsulfide te verwijderen.
gebruik
waterstofsulfide wordt voornamelijk gebruikt voor de productie van zwavelzuur en zwavel. Het wordt ook gebruikt om een verscheidenheid van anorganische sulfiden tot stand te brengen die worden gebruikt om pesticiden, leer, kleurstoffen en geneesmiddelen tot stand te brengen. Waterstofsulfide wordt gebruikt om zwaar water te produceren voor kerncentrales (zoals CANDU reactoren specifiek). Waterstofsulfide kan ook worden gebruikt in de landbouw als ontsmettingsmiddel. Het wordt ook veel gebruikt in chemische analyse.,
Ijzersmelters, stortplaatsen, voedselverwerkende bedrijven en brouwerijen zijn enkele voorbeelden van industriële bronnen die waterstofsulfide produceren of gebruiken. Het gas moet op de juiste wijze worden verwijderd omdat de uitstoot van waterstofsulfide gevaarlijk kan zijn.
gezondheidseffecten
de gezondheidseffecten van inademing van waterstofsulfide hangen af van de hoeveelheid waaraan een persoon wordt blootgesteld. Waterstofsulfide is zelfs in relatief kleine concentraties gevaarlijk omdat het zowel irriterend als verstikkend werkt. Bij relatief lage concentraties irriteert waterstofsulfide de ogen, neus en keel., Deze effecten zijn vooral gevaarlijk voor kinderen en mensen met een verminderde longfunctie.
bij bepaalde concentraties kan blootstelling aan waterstofsulfide resulteren in bewusteloosheid in een paar ademhalingen of bijna onmiddellijk overlijden. In concentraties zo laag als 500-700 ppm, waterstofsulfide kan leiden tot de dood binnen een uur. Bij concentraties van slechts 1000-2000 ppm kan waterstofsulfide bijna onmiddellijk de dood veroorzaken. Gezondheidseffecten van blootstelling zijn hoofdpijn, geheugenverlies en problemen met het cardiovasculaire systeem., Herhaalde blootstelling aan waterstofsulfide kan leiden tot oogontsteking, vermoeidheid, prikkelbaarheid, slapeloosheid en gewichtsverlies.
voor verdere uitlezing
- Gas
- Aardgas
- aardolie
- koolmonoxide
- chemische
- of bekijk een willekeurige pagina
Geef een reactie