FOTOBIOLOGIA soczewki ludzkiej
Joan E. Roberts
Fordham University, Department of Natural Sciences
113 West 60th Street, New York City, NY 10023
iv id=”bc8f04aeac”
wprowadzenie
podstawową funkcją ludzkiej soczewki jest skupienie światła niezakłóconego na siatkówce. Podczas gdy właściwości transmisyjne większości składników oka są stabilne, właściwości transmisyjne soczewki zmieniają się przez całe życie, jak widać na rysunku 1.,
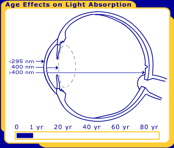
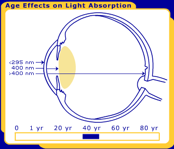
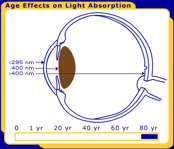
rysunek 1. Zmiany w ludzkiej soczewce przez całe życie. Na zdjęciu są po urodzeniu, 40 lat i 80 lat.
ekspozycja na intensywne światło słoneczne może stanowić szczególne zagrożenie dla soczewki oka i prowadzić do powstania zaćmy, która upośledza widzenie., Zarówno ekspozycja UV-A, jak i UV-B są głównymi czynnikami ryzyka indukcji zaćmy, zwłaszcza u osób powyżej 70 roku życia, ponieważ z wiekiem zdolność oka do ochrony przed uszkodzeniem światłem jest zagrożona. Ekspozycja na promieniowanie UV od odbicia wody, piasku lub śniegu jest szczególnie szkodliwe dla soczewki oka. oprócz promieniowania UV sam, istnieje wiele barwników, leków i leków ziołowych, które w obecności światła widzialnego i promieniowania UV może wywołać zaćmę . Ta fototoksyczna reakcja powoduje bardzo wczesną zaćmę .,
wszelkie zmiany w klarowności soczewki pogorszą jakość obrazu prezentowanego siatkówce i w znacznym stopniu wpłyną na percepcję wzrokową. W tym module dowiemy się o fotochemii i fotobiologii soczewki oraz o tym, jak te właściwości wpływają nie tylko na siatkówkę, ale na ogólne zdrowie człowieka .
struktura przedniej części oka (segmentu przedniego)
ludzkie oko składa się z kilku przedziałów, jak widać na rysunku 2. Najbardziej zewnętrzna warstwa zawiera twardówki, której funkcją jest ochrona gałki ocznej, i rogówki, która skupia światło przychodzące na soczewce., Pod tą warstwą znajduje się naczyniówka zawierająca tęczówkę, która jest znana jako uvea. Region ten zawiera melanocyty, które zawierają melaninę pigmentową, której funkcją jest zapobieganie rozpraszaniu światła. Otwór w tęczówce, źrenica, rozszerza się i kurczy, aby kontrolować ilość przychodzącego światła. Tęczówka i soczewka są skąpane w cieczy wodnistej. Wodny humor jest płynem, który służy jako przezroczysty układ krążenia (co przepływ krwi robi w tkankach nieprzezroczystych)., Nie tylko utrzymuje ciśnienie wewnątrzgałkowe, ale także zapewnia odżywianie soczewki i rogówki oraz usuwa zanieczyszczenia i odpady z tych tkanek oka. Wodnisty humor zawiera wysokie stężenia różnych przeciwutleniaczy. Obiektyw jest umieszczony za przesłoną. Funkcją soczewki jest skupienie światła niezakłóconego na siatkówce, która znajduje się w tylnej części oka (segment tylny) .

Rysunek 2. Struktura ludzkiego oka.,
struktura ludzkiej soczewki
struktura ludzkiej soczewki jest widoczna na rysunku 3. Soczewka jest przezroczystym narządem znajdującym się za rogówką i tęczówką . Zewnętrzna krawędź soczewki składa się z pojedynczej warstwy komórek nabłonkowych i błony pokrywającej cały narząd . Komórki nabłonka soczewki nie dzielą się, chyba że są poddawane naprawie. Niektóre komórki nabłonkowe tracą swoje jądra i inne organelle i stają się komórkami włókien soczewkowych . Te komórki włókien soczewki są wypełnione 30% roztworem białka, znanego jako cytosol (rozpuszczalne) białka soczewki., Ponieważ w komórkach włókien soczewki występuje niewielki obrót białka, uszkodzenie białka soczewki gromadzi się przez całe życie.

Rysunek 3. Struktura ludzkiej soczewki.
szew i równik to terminy anatomiczne w okulistyce. Szew oznacza szwy soczewki. Wzory szwów stają się bardziej złożone, ponieważ więcej warstw włókien soczewki są dodawane do zewnętrznej części soczewki. Równik oznacza krawędź największej części soczewki (podobnie jak równik na kuli ziemskiej).,
kiedy światło jest szkodliwe dla ludzkiej soczewki?
chociaż światło środowiskowe jest w większości łagodne, istnieje kilka warunków, w których narażenie na światło środowiskowe staje się szkodliwe. Aby określić, czy światło jest szkodliwe, należy wziąć pod uwagę następujące czynniki: intensywność, długość fali, miejsce uszkodzenia, napięcie tlenu, chromofory, systemy obronne i mechanizmy naprawcze.
intensywność. Im większa intensywność światła, tym bardziej prawdopodobne jest uszkodzenie oka. Światło, które zwykle nie może być szkodliwe, może wyrządzić ostre szkody, jeśli jest wystarczająco intensywne., Na przykład wiadomo, że oko może zostać uszkodzone (tymczasowo lub na stałe) przez ekspozycję na światło słoneczne odbijające światło od śniegu (ślepota śnieżna) lub przez wpatrywanie się w słońce podczas zaćmienia . Następuje wzrost promieniowania UV wraz z rozrzedzeniem ochronnej warstwy ozonowej . Podobnie, oko może wytrzymać uszkodzenia ze sztucznych źródeł światła, które emitują UV-A lub UV-B. Skumulowane uszkodzenia świetlne wynikają z mniej intensywnej ekspozycji przez dłuższy okres czasu i często są wynikiem utraty ochrony związanej z wiekiem .
, Promieniowanie otoczenia, ze słońca lub ze sztucznych źródeł światła, zawiera różne ilości światła UV-C (100-280 nm), UV-B (280-315 nm), UV-A (315-400 nm) i widzialnego (400-700 nm). Im krótsza długość fali, tym większa energia, a zatem większy potencjał uszkodzeń biologicznych. Jednak, chociaż dłuższe fale są mniej energiczne, wnikają głębiej w oko .
Aby doszło do reakcji fotochemicznej, światło musi zostać pochłonięte w określonej tkance ocznej., Oko naczelne / ludzkie ma unikalne właściwości filtrujące, które określają, w którym obszarze oka każda długość fali światła zostanie pochłonięta. Promieniowanie UV poniżej 295 nm jest filtrowane od dotarcia soczewki przez ludzką rogówkę. Oznacza to, że najkrótsze, najbardziej energetyczne długości fal światła (wszystkie UV-C i niektóre UV-B) są filtrowane, zanim dotrą do ludzkiej soczewki. Większość światła UV jest absorbowana przez soczewkę, ale dokładny zakres długości fali zależy od wieku. U dorosłych soczewka pochłania Pozostałe UV-B i całe UV-a (295-400 nm), a zatem tylko światło widzialne dociera do siatkówki., Jednak bardzo młoda ludzka soczewka przepuszcza małe okno światła UV-B (320 nm) do siatkówki, podczas gdy starsza soczewka filtruje większość krótkiego niebieskiego światła widzialnego (400-500 nm). Transmisja różni się również od gatunku; soczewki ssaków innych niż naczelne przekazują do siatkówki promieniowanie UV dłuższe niż 295 nm .
miejsce lekkich uszkodzeń obiektywu. Soczewka składa się z dwóch części, które są najbardziej podatne na uszkodzenia: (zewnętrzne) komórki nabłonkowe i (wewnętrzna) błona włókien. Komórki nabłonkowe kontrolują transport do soczewki., Mają bezpośredni kontakt z cieczą wodną i są najbardziej narażone na uszkodzenia fototoksyczne. Uszkodzenie tych komórek z łatwością zagrozi żywotności soczewki . Błona włóknista może być uszkodzona fotochemicznie przez uszkodzenie lipidów i / lub głównego wewnętrznego białka błonowego .
reakcje fototoksyczne mogą prowadzić do modyfikacji DNA i niektórych aminokwasów (histydyny, tryptofanu, cysteiny) i/lub kowalencyjnego przywiązania uczulacza do białek soczewki cytozolu ., Chromofory związane kowalencyjnie mogą wtedy działać jako endogenne substancje uczulające i wytwarzać długotrwałą wrażliwość na światło. Ponadto dochodzi do niefotochemicznie indukowanej modyfikacji białek soczewek związanych z cukrzycą . Stwierdzono, że wysokie stężenie glukozy prowadzi do glikozylacji epsilon-aminowych grup reszt lizyny. Wszystkie te rodzaje uszkodzeń spowodują zmianę współczynnika załamania materiału soczewki, prowadząc do agregacji i ostatecznie zmętnienia (kataraktogenezy) ., Niedawno opracowana technika (ScanTox) mierzy bardzo wczesne zmiany w jakości optycznej (ogniskowania) soczewki, nawet zanim uszkodzenie spowoduje zmętnienie soczewki .
chromofory. Chromofor jest substancją pochłaniającą światło. Chromofor oczny może być endogennym Związkiem naturalnie występującym w oku lub egzogennym środkiem, który przeszedł przez bariery krew-oczne i przeniknął do określonego miejsca. Aby światło mogło uszkodzić soczewkę, światło musi najpierw zostać pochłonięte przez chromofor znajdujący się w jakiejś komorze soczewki.,
a) endogenne (naturalnie występujące) chromofory w ludzkiej soczewce. Chromofory w ludzkiej soczewce zmieniają się przez całe życie, jak widać na rysunku 4a i b. w rzeczywistości jest niewiele uszkodzeń ludzkiego oka od światła przed wiekiem średnim. Dzieje się tak, ponieważ Dorosła ludzka soczewka zawiera żółte chromofory (3-hydroksykureniny), które pochłaniają światło, ale uwalniają energię, zanim będzie miała szansę na wyrządzenie jakichkolwiek szkód ., Tak więc chromofory kynureninowe obecne w soczewce dorosłego człowieka są nie tylko bezpieczne, ale służą do ochrony siatkówki poprzez filtrowanie promieniowania UV, zapobiegając w ten sposób dotarciu i uszkodzeniu siatkówki . Po średnim wieku enzym (aminotransferaza kynurenina), wytwarzany w coraz większych ilościach, przekształca chromofory ochronne (3-OH kynurenina i jej glukozyd) w niszczące chromofory, kwas ksanturenowy i glukozyd ksanturenowy . Gdy te związki ksantureniczne absorbują światło, wytwarzają reaktywne formy tlenu (tlen singletowy i / lub ponadtlenek), które uszkadzają białka soczewek ., Inny chromofor, N-formyl kynurenina, utworzony z ciągłego fotooksydacji endogennego tryptofanu, również wytwarza tlen singletowy i ponadtlenek, który uszkadza białka soczewek . Tak więc kwas ksanturenowy i N-formyl kynurenina są prawdopodobnie kandydatami na chromofory odpowiedzialne za tworzenie się zaćmy związanej z wiekiem.

rysunek 4a. zmiany związane z wiekiem w ludzkiej soczewce. W miarę starzenia się soczewki chromofory zmieniają kolor ludzkiego oka z przezroczystego (środkowy) na żółty (u góry po prawej)., W wyniku zmian starzenia w ludzkiej soczewce występuje zmętnienie soczewki, które jest znane jako zaćma (lewy górny róg). Soczewki krów (spód) i innych naczelnych mają jasne soczewki przez całe życie.
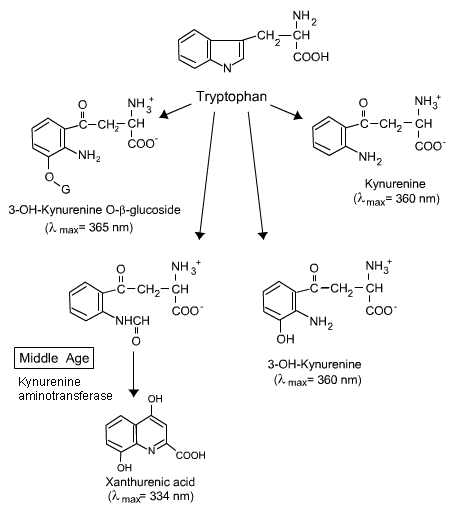
rysunek 4b. wieku. Zwróć uwagę na zmianę W Średnim Wieku. Więcej informacji można znaleźć w tekście powyżej.
b) ksenobiotyki lub egzogenne chromofory w soczewce., Intensywne lub nagromadzone promieniowanie UV-B lub UV-A powoduje bezpośrednie uszkodzenie ludzkiej soczewki. Jednak w obecności światła aktywowanego (światłoczułe) lek, leki ziołowe, (hyperycyna w dziurawiec) lub nanocząstki, pacjenci są w niebezpieczeństwie wzmocnionego urazu oka od promieniowania UV otoczenia i światła widzialnego ., Stopień, w jakim dana substancja chemiczna jest zdolna do wytwarzania fototoksycznych efektów ubocznych w oku, zależy od kilku parametrów, w tym: 1) struktury chemicznej; 2) widma absorpcji leku; 3) wiązania leku z tkanką oczną; i 4) zdolność do przekraczania barier krew-Oczy.
każdy związek o strukturze pierścienia trójcyklicznego, heterocyklicznego lub porfirynowego jest potencjalnym chromoforem ocznym, jeśli ma absorbancję powyżej odcięcia rogówki (>295 nm). Kiedy te egzogenne (zewnętrzne) substancje uczulające wiążą się z tkankami ocznymi (tj.,, białka soczewek), wydłużony jest ich czas retencji w soczewce, a potencjalne zagrożenie, jakie stwarzają, jest zwiększone. Substancje amfifilowe lub lipofilowe są w stanie przekroczyć większość barier soczewkowych . Soczewka jest zasilana wodnym humorem i stosunkowo trudno jest substancji przejść przez wodny humor do soczewki przez spożycie. Jednak, gdy w obiektywie, jest również trudne do usunięcia substancji obcych.
napięcie tlenu. Napięcie tlenu w obiektywie jest bardzo niskie, ale jest wystarczające do wystąpienia fotooksydacji .
systemy obronne., Obiektyw posiada bardzo skuteczny system obrony przed uszkodzeniem światłem i promieniowaniem. Soczewka zawiera enzymy przeciwutleniające (dysmutaza ponadtlenkowa (SOD) i katalaza) oraz przeciwutleniacze (witamina E, C, luteina, glutation), które służą do ochrony przed uszkodzeniami oksydacyjnymi i fotoindukcyjnymi . Niestety większość z tych przeciwutleniaczy i enzymów ochronnych zmniejsza się już w wieku czterdziestu lat, pozostawiając soczewkę bezbronną przed lekkimi uszkodzeniami.
Naprawa., Komórki nabłonka soczewki obwodowej są zdolne do naprawy wiązań DNA indukowanych promieniowaniem UV-B (dimery cyklobutanu pirymidyny i 6-4 pirymidyny-pirymidonu), ale każda dodatkowa ekspozycja na UV-A zakłóca naprawę komórek. Ze względu na niewielką rotację białek soczewek dochodzi do uszkodzenia białek soczewek.
mechanizm uszkodzenia Światła Obiektywu
Fotooksydacja. Intensywne światło może wywołać bezpośrednie uszkodzenie DNA, ale przy mniej intensywnym świetle oko jest uszkodzone w wyniku reakcji fototoksyzacji., W reakcjach fotooksydacji chromofor w oku pochłania światło i utlenia niektóre aminokwasy i / lub kwasy nukleinowe, co powoduje uszkodzenie całej soczewki. Chromofor może być endogenny (naturalny) lub egzogenny (lek, leki ziołowe lub nanocząstki, które nagromadziły się w oku). Absorpcja światła pobudza chromofor do wzbudzonego stanu singletowego, który następnie przechodzi krzyżowanie międzysystemowe i osiąga stan potrójny., W stanie triplet chromofor następnie przechodzi przez typ i (wolne rodniki) lub typ II (singletowy tlen), aby spowodować ewentualne uszkodzenie . Fotooksydacja może wystąpić w obiektywie za pomocą mechanizmu typu i lub typu II, lub obu jednocześnie.
chromofory to Dorosła ludzka soczewka może być wzbudzona przez światło, ale z tego stanu wzbudzonego (singlet) schodzą bardzo szybko (nanosekundy), więc nie mają szans na osiągnięcie stanu potrójnego, na uszkadzanie aktywnych półproduktów, a tym samym na spowodowanie uszkodzenia soczewki ., Jednak, gdy skuteczne fotouczulacze, kwas ksanturenowy, glukozyd i N-formyl kynurenina są obecne w soczewce, a soczewka jest narażona na promieniowanie UV, są one w stanie wytwarzać trojaczki z wystarczającą wydajnością (wydajność kwantowa), aby utworzyć reaktywne formy tlenu i wolne rodniki, które z kolei uszkadzają tkankę soczewki.
zaćma
Mechanizm indukcji. Ludzka soczewka jest zwykle przezroczysta do wieku 40 lat. Ta przezroczystość jest wynikiem uporządkowanego ułożenia włókien białkowych w soczewce normalnie ., W średnim wieku traci się naturalną ochronę enzymatyczną i antyoksydacyjną oka przed promieniami UV – A i UV-B, a jednocześnie zwiększa się produkcja fotochemicznie aktywnych chromoforów. Ponieważ soczewka pochłania światło otoczenia, te chromofory są fotoaktywowane i wytwarzają reaktywne formy tlenu, takie jak tlen singletowy i ponadtlenek. Białka soczewki (alfa, beta, gamma krystaliny) ulegają denaturacji, lub komórki nabłonka soczewki nie są już w stanie naprawić uszkodzeń spowodowanych światłem otoczenia ., W wieku 70 lat soczewka w końcu staje się wystarczająco mętna, aby utrudnić widzenie, a osoba mówi się, że ma zaćmę związaną z wiekiem (ryc. 4a) .
zaćma może również rozwinąć się w znacznie wcześniejszym wieku, gdy osoba jest narażona na nadmierne promieniowanie UV, dym papierosowy i zanieczyszczenie powietrza, leki fotouczulające, sterydy lub ma cukrzycę. Podstawową przyczyną tych zaćmy jest również oksydacyjne (i fototoksyczne) uszkodzenia komórek nabłonka soczewki i białek soczewki.,
utrzymanie integralności strukturalnej jest szczególnie ważne dla Alfa-krystaliny białka soczewkowego ze względu na jego rolę jako opiekuna molekularnego. Alfa-Krystalina jest agregatem dwóch polipeptydów, A i B, które są małymi białkami szoku cieplnego, które zapobiegają agregacji białek indukowanych przez promieniowanie UV (A i B). Dodając i usuwając produkcję Alfa-krystaliny z komórek nabłonka soczewki i wykazując, że alfa-krystalina zapewnia naturalną ochronę przed uszkodzeniem komórek soczewki promieniowaniem UV . Alfa-Krystalina chroni również przed promieniowaniem UV-a hamującym aktywność enzymu ochronnego (katalazy)., Specyficzne miejsca uszkodzenia Alfa-krystaliny zarówno z endogennymi, jak i egzogennymi chromoforami zostały wykryte przy użyciu spektrometrii mas i technik przeciwciała monoklonalnego . Zaawansowane produkty końcowe glikacji Znalezione w zaćmy cukrzycowej mogą również zachowywać się jak fotouczulacze i utleniać białka soczewki .
wszystkie endogenne lub egzogenne utlenianie denaturuje białka soczewki, zmniejsza ich rozpuszczalność, a ostatecznie powoduje utratę przezroczystości w soczewce, co jest znane jako zaćma., Zaćma, która występuje w centralnej części soczewki jest znany jako zaćma jądrowa, a te, które występują na obrzeżach soczewki są znane jako zaćma korowa. Rzadsza forma zaćmy jest znana jako tylna zaćma subkapsularna. Zaćma ta jest na ogół uważana za genetycznie powiązaną i występuje po urodzeniu lub bardzo wczesnym wieku, lub w wyniku stosowania sterydów lub cukrzycy .
Diagnostyka i leczenie., Zaćma może być łatwo zdiagnozowana za pomocą „lampy szczelinowej” lub oftalmoskopu, który bada soczewkę pod kątem braku przezroczystości i określa lokalizację i gęstość zmętnienia. Ponadto, test ostrości wzroku określi, jak dobrze pacjent może zobaczyć z zaćmy. Gdy zauważono znaczną utratę wzroku, leczenie polega na chirurgicznym usunięciu soczewki. Soczewka ta jest powszechnie zastępowana wewnątrzgałkową soczewką z tworzywa sztucznego zawierającą filtr UV – A i UV-B, aby zastąpić moc ogniskowania i filtrowania utraconą podczas usuwania soczewek zaćmy ., Ostatnio wewnątrzgałkowe sztuczne soczewki są dostępne z krótkimi filtrami światła niebieskiego (400-440 nm), które są ważne dla ochrony osób starszych przed zwyrodnieniem plamki żółtej i cukrzycą przed retinopatią cukrzycową .
profilaktyka. Jeśli zapobiec światło z ekscytujących endogennych lub egzogennych chromoforów w obiektywie, lub zablokować uszkodzenia reaktywnych form tlenu z przeciwutleniaczami, może zapobiec lub opóźnić zaćmy z formowania .
A) Okulary przeciwsłoneczne . Zarówno UV – A, jak i UV-B nie są konieczne ani do widzenia, ani do wywołania odpowiedzi okołodobowej., Z drugiej strony, zarówno UV – A jak i UV-B indukują powstawanie zaćmy. Usunięcie tych długości fal z ekspozycji ocznej znacznie zmniejszy ryzyko wczesnego powstawania zaćmy. Można to łatwo zrobić, nosząc okulary przeciwsłoneczne, które blokują fale poniżej 400 nm . Jednak ze względu na geometrię oka okulary te muszą być okularowymi okularami przeciwsłonecznymi, aby zapobiec przedostawaniu się do oka odblaskowego promieniowania UV.
b) przeciwutleniacze ponieważ wiek zmniejsza normalną produkcję przeciwutleniaczy w soczewce, zwiększenie jedzenia owoców i warzyw zostało zasugerowane, aby zastąpić brakującą ochronę ., Ponadto wykazano, że suplementacja witaminami i przeciwutleniaczami, w tym witaminą E i luteiną, jest szczególnie skuteczna w opóźnianiu zaćmy związanej z wiekiem .
suplementy powinny być zbilansowane, ponieważ szkodliwe reakcje utleniania mogą wystąpić, jeśli przyjmowany jest tylko jeden przeciwutleniacz . W badaniu AREDS (Age-Related Eye Disease Study) sponsorowanym przez National Eye Institute stwierdzono, że nadmierny beta-karoten był związany ze zwiększonym ryzykiem raka płuc u palaczy, podczas gdy nadmierny Zn był związany ze zwiększonym ryzykiem raka prostaty., Ponieważ luteina, a nie beta-karoten, jest naturalnym karotenoidem występującym w soczewce i siatkówce, suplementacja nadmiernym beta-karotenem jest nie tylko niepotrzebna, aby chronić oko,ale jest niebezpieczna dla palaczy i byłych palaczy. Inne naturalne produkty, takie jak zielona herbata, która zawiera polifenole (galusan epigallokatechiny) i Ashwagandha (korzeń Withania somnifera) stosowane w tradycyjnej medycynie ajurwedyjskiej wykazano również opóźnić światło wywołane uszkodzenie soczewki .
wnioski
powstawanie zaćmy jest chorobą związaną z wiekiem. Większość ludzi stworzy zaćmę do czasu, gdy mają 70 lat., Zarówno UV-A jak i UV-B są bardzo ważnymi czynnikami ryzyka rozwoju wczesnej zaćmy. Ponadto ekspozycja na nawet światło widzialne w obecności steroidów, leków fotouczulających, kosmetyków i nanocząstek może znacznie zwiększyć ryzyko wczesnej zaćmy. Unikanie promieniowania UV Za pomocą odpowiednich okularów przeciwsłonecznych oraz odpowiednia kombinacja utleniających i redukujących przeciwutleniaczy może pomóc opóźnić lub wyeliminować to oślepiające zaburzenie u osób starszych.
Andley UP (2008) the lens epithelium: focus on the expression and function of the alpha-crystallin chaperones., Int J Biochem Cell Biol. 40:317-23.
Andley UP (2007) Krystaliny w oku: Funkcja i patologia. Prog Retin Eye Res. 26: 78-98.
Andley U P, Rhim JS , Chylack Jr LT, Fleming TP (1994) Propagation and immortalization of human lens epithelial cells, Invest. Ophthalmol. Vis. Sci., 35:3094-3102.
Andley UP, Patel HC, Xi JH, Bai F (2004) Identification of genes responsive to UV-a radiation in human lens epithelial cells using cDNA microarrays. Fotochem. Fotobiol. 80, 61-71.,
Andley UP, Song Z, Mitchell DL (1999) DNA repair and survival in human lens epithelial cells with extended lifespan. Curr Eye Res. 18: 224-30.
Argirov OK, Lin B, Ortwerth BJ (2004) J. Biol. Chem. 279:6487-6495.
Argirova MD, Breipohl w (2002) Wolny Radic. Res. 36:1251-1259.,
Ayala MN, Michael R, Soderberg PG (2000) Influence of exposure time for UV radiation-induced cataract Invest Ophthalmol Vis Sci. 41: 3539-43. Bachem, A. (1956). Ophthalmic action spectra. Am. J. Ophthalmol. 41: 969-975.
Balasubramanian D (2000) J. O. Pharmacol. Therap. 16, 285-297.
Balasubramanian D (2005) Photodynamics of Cataract: An Update on endogenne Chromophores and Antioxidants . Fotochem. Fotobiol. 81:498-501.
Benedek GB (1971) teoria przezroczystości oka. Appl. Optyka 10:459-473.,
Bochow TW, West SK, Azar A, Munoz B, Sommer A, Taylor H R (1989) Ophthalmology 107: 369-372.
Barker, FM, Brainard GC and Dayhaw-Barker P (1991) transmitancja ludzkiej soczewki jako funkcja wieku. Inwestuj. Ophthalmol. Vis. Sci. 32S str. 1083.
Bassnett S I Mataic D (1997) Chromatin Degradation in Differentiating Fiber Cells Of The Eye Lens J. Cell Biol. 137: 37-49.,
Busch M, Gorgels TG, Roberts JE, van Norren D (1999) the effects of two stereoisomers of N-acetylocysteine on photochemical damage by UVA and blue light in rat retina. Fotochem. Fotobiol. 70:353-358.
Coroneo MT (1990) stężenie Albedo w oku przednim: zjawisko lokalizujące niektóre choroby słoneczne. Okulistyczny. / Align = „center” / 2,6066
Dillon J and Atherton SJ (1990) Time Resolved Spectroscopic Studies on the until Human Lens. Fotochem. Fotobiol. 51 :465-468.
Dillon J (199) Fotofizyka i Fotobiologia oka. J. Fotochem.Fotobiol. B BioI. 10:23-40.,
Dovrat A, Sivak JG (2005) Long-term lens organ Cult system with a method for monitoring lens optical quality. Fotochem Fotobiol. 81:502-505.
Edge R, Land EJ, McGarvey DJ, Mulroy L, Truscott TG (1998) Relative one-electron reduction potentials of carotenoid radical cations and the interactions of carotenoids with the vitamin E radical cation. J. Am. Chem. Soc. 120:4087-4090.
Edge R, McGarvey DJ, Truscott TG (1997) the carotenoids as anti-oxidants-a review. J. Fotochem. Fotobiol. B: Biol. 41:189-200.
Falkner-Radler CI, Benesch T, Binder S., (2008) Blue light-filter intraocular lenses in witrectomy combined with cataract surgery: results of a randomized controlled clinical trial.Am J Ophthalmol. 145:499-503.
Finley EL, Dillon J, Crouch RK, Schey KL (1998). Identyfikacja produktów tryptofanu w utlenianiu bydlęcej Alfa-Krystaliny. Białko Sci., 7:2391-2397.
Finley EL, Dillon J, Crouch RK, Schey KL (1998) Radiolysis-induced oxidation of bovine alpha-crystallin. Fotochem. Fotobiol. 68:9-15.
Finley EL, Busman M, Dillon J, Crouch RK, Schey KL (1997) Identification of photooxidation sites in bovine alpha-crystallin., Fotochem. Fotobiol. 66:635-641.
Giblin FJ (2000) Glutation: a Vital Lens Antioxidant. J. Ocul. Farmakol. Ther. 16: 121-135.
Horwitz J, Zigman S (1997) czy Alfa-krystaliny chronią katalazę przed uszkodzeniami UV? Biol Bull. 193:254-255.
Jacques PF, Chylack LT Jr, Hankinson SE, Khu PM, Rogers G, Friend J, Tung w, Wolfe JK, Padhye N, Willett WC, Taylor A. (2001). Arch Ophthalmol. 119:1009-1019.,
Khachik F, Bernstein PS, Garland DL (1997) Identification of luteina and zeaksanthin oxidation products in human and monkey retinas. Inwestuj. Ophthalmol. Vis. Sci. 38 s. 1802-1811.
Krishna CM, Uppuluri S, Riesz P, Zigler Jr JS, Balasubramanian D (1991) A Study of the Photodynamic Efficienties of Some eye Lens Components. Fotochem. Fotobiol. 54:51-58.
Kuszak JR, Peterson KL, Sivak JG, Herbert KL. (1994) the interrelationship of lens anatomy and optical quality. II. soczewki Prymasowskie. Exp Eye Res. 59: 521-35.,
Kwan M, Niinikoske J, Hunt TK (1971) napięcie tlenu w wodzie i soczewce. Inwestuj. Ophthalmol. 11:108-111.
Lyle BJ, Mares-Perlman JA, Klein BE, Klein R, Greger JL (1999) Am. J. Epidemiol. 149:801-809.
Malina HZ, Martin XD (1996) powstawanie pochodnych kwasu Ksanturenowego w soczewce jest odpowiedzialne za zaćmę starczą u ludzi. Graefes Arch. Clin. Exp.Ophth., 234: 723-730
McLaren JW, Dinslage S, Dillon JP, Roberts JE, Brubaker RF (1999) pomiar napięcia tlenu w przedniej komorze królików. Inwestuj. Ophthalmol. Vis. Sci. 39:1899-1909.
Merriam JC (1996) the Concentration of Light in The Human Lens . Trans.Am. Ophthalmol. Soc. 94: 803-918.
Norval M, Cullen AP, de Gruijl FR, Longstreth J, Takizawa Y, Lucas RM, Noonan FP, van der Leun JC. (2007). Wpływ stratosferycznego zubożenia ozonu na zdrowie człowieka i jego interakcje ze zmianami klimatycznymi. Fotochem Fotobiol Sci. 6:232-51.,
Olmedilla B, Granado, F, Blanco I, Vaquero M (2003) Luteina, ale nie alfa-tokoferol, suplementacja poprawia funkcje wzroku u pacjentów z zaćmy związanej z wiekiem: 2-letnie, podwójnie ślepe, kontrolowane placebo badanie pilotażowe. Żywienie 19, 21-24
Roberts JE (2008) „Drug Induced Ocular Phototoxicity” In: Marzulli and Maibach ' s Dermatotoxicology, 7th Edition, edited by H. Zhai, K-P Wilhelm, and H. Maibach, Chapter 28, pp 269-278. Taylor & Francis Group, Boca Raton, Floryda.
Roberts JE, Wielgus AR, Boyes WK, Andley U, Chignell CF ., (2008) Phototoxicity and cytotoxicity of fullerol in human lens epithelial cells. Toxicology and Applied Pharm 228:49-58.
Roberts JE (2002) Screening for Ocular Phototoxicity. International Journal of Toxicology 21:491-500.
Roberts JE, Finley EL, Patat SA, Schey K L (2001) Photooxidation of Lens Proteins with Xanthurenic Acid: A Putative Chromophore for Cataractogenesis. Photochem. Photobiol. 74: 740-744.
Roberts JE. (2001) Ocular phototoxicity. J. Photochem. Photobiol. B: Biology 64, 136-143.,
Roberts JE, Wishart JF, Martinez L Chignell CF (2000) Photochemical Studies on Ksanturnic Acid. Fotochem. Fotobiol. 72: 467471.
Roberts JE (2000) Light and Immunomodulation. NY Acad Sci. 917:435-445.
Roberts JE, Roy D, Dillon J (1985) the photosensitized oxidation of the calf lens main intrinsic protein (MP26) with hematoporphyrin. Curr. Eye Res. 4: l8l-185.
Rodriguez-Galietero A, Montes-Mico R, Munoz G, Albarran-Diego C. (2005) blue-light filtering intraocular lens in patients with diabetes: contrast sensitivity and chromatic discrimination. Operacja Załamania Katarakty J., 31:2088-2092.
Samiec PS, Drews-Botsch C, Flagge EW, Kurtz JC, Sternberg P, Reed RL Jones DP (1998) glutation in human plasma declines in association of aging, age-related macular degeneration and diabetes. Wolny Radic. Biol. Med. 24:699-704.
Schalch w I Chylack LT Jr, (2003). przegląd i porównanie badań Ards i REACT cataract. Ophthalmologe 100, 181-189.
Schey KL, Little m, Fowler JG, Crouch RK (2000) Characterization of human lens major intrinsic protein structure, Invest. Oftal. Vis Sci., 41 175-182.,
Schey KL, Patat S, Chignell CF, Datillo M, Wang RH, Roberts JE (2000) Photooxidation of lens proteins by hyperycin (active ingredient in St.John ' s Wort). Fotochem. Fotobiol. 72:200-207.
Seth RK, Kharb S (1999) Protective Function of Alpha-tokoferol Against the Process of Cataractogenesis in Humans. Ann. Nutr. Metab. 43: 286-289.
Sliney DH (2007) komentarz : widmowa transmisja IOL wyrażona jako epoka wirtualna. Br J Ophthalmol. 91:1261-1262.
sliney DH (2005) geometria ekspozycji i środowisko widmowe determinują wpływ fotobiologiczny na ludzkie oko. Fotochem Fotobiol., 81:483-489.
Sliney, D. H. (1997). Optical radiation safety of medical light sources. Phys. Med. Biol. 42:981-996.
Straight R, Spikes JD (1985) Photosensitized oxidation of biomolecules. W: O. Singlet, Editor, A. A. Frimer, Editor, Polymers and Biopolimers Vol. 2012-01-14 14: 00: 00
Staniszewska MM, Nagaraj RH . (2005) 3-hydroxykynurenine-mediated modification of human lens proteins: structure determination of a major modification using a monoclonal niwecznik. J Biol Chem. 280:22154-64.,
Thiagarajan G, Venu T, Balasubramanian D (2003). Curr. Sci. 85, 1065-1071.
Thiagarajan G, Shirao E, Ando K, Inoue A, Balasubramanian D (2002) Fotochem. Fotobiol. 76, 368-372.
van Norren D, van de Kraats J. (2007) Spectral transmission of intraocular lens expressed as a virtual age. Br J Ophthalmol; 91: 1374-1375.,
Yeum KJ, Shang FM, Schalch WM, Russell RM, Taylor a (1999) fat-soluble nutrient concentrations in different layers of human cataractous lens. Curr.Eye Res. 19: 502-505.
Zigman S, McDaniel T, Schultz J, Reddan J (2000) Effects of intermittent UVA exposure on cultured lens epithelial cells. Current Eye Res. 20: 95-100
Zigman S, Rafferty NS, Rafferty KA, Lewis n (1999) wpływ polifenoli zielonej herbaty na stres fotooksydacyjny soczewki. Biol-Bull. 197: 285-286.
Zigman S (2000) Lens UVA photobiology. J Ocul Pharmacol Ther. 16:161-165.
Dodaj komentarz