cel nauki
- omów właściwości azotu.
kluczowe punkty
- azot jest pierwiastkiem chemicznym o symbolu N i liczbie atomowej 7. Azot elementarny jest bezbarwnym, bezwonnym, pozbawionym smaku i w większości obojętnym gazem dwuatomowym w standardowych warunkach, stanowiącym 78,09 procent objętości atmosfery ziemskiej.,
- Gaz azotowy jest gazem przemysłowym wytwarzanym przez frakcyjną destylację ciekłego powietrza lub za pomocą środków mechanicznych przy użyciu powietrza gazowego. Azot komercyjny jest często produktem ubocznym przetwarzania powietrza w celu przemysłowego zagęszczania tlenu.
- Gaz azotowy ma wiele zastosowań, w tym służy jako obojętny zamiennik powietrza, w którym utlenianie jest niepożądane. Ciekły azot jest również używany do kriogenicznego zamrażania obiektów.
terminy
- elementalOf, odnoszący się lub będący elementem (w przeciwieństwie do Związku).,
- aminokwasgeneralnie, cząsteczki, które zawierają zarówno aminową, jak i karboksylową grupę funkcyjną kwasu. Monomery, z których zbudowane są łańcuchy polipeptydowe lub białka, to aminokwasy.
- nitrogenowy pierwiastek chemiczny (symbol N) o liczbie atomowej 7 i masie atomowej 14,0067 UAM.
pierwiastek azot został odkryty jako oddzielny składnik powietrza przez szkockiego lekarza Daniela Rutherforda w 1772 roku. Związki azotowe były dobrze znane w średniowieczu. Alchemicy znali kwas azotowy jako aqua fortis (mocna woda)., Mieszanina kwasów azotowych i solnych była znana jako aqua regia (woda Królewska), słynąca ze swojej zdolności do rozpuszczania złota (król metali). Do najwcześniejszych zastosowań wojskowych, przemysłowych i rolniczych związków azotowych używano saletry (azotanu sodu lub azotanu potasu), głównie w prochu, a później jako nawozu.
azot jest pierwiastkiem chemicznym o symbolu N i liczbie atomowej 7. Azot elementarny jest bezbarwnym, bezwonnym, pozbawionym smaku i w większości obojętnym gazem dwuatomowym w standardowych warunkach, stanowiącym 78,09 procent objętości atmosfery ziemskiej., Azot jest powszechnym pierwiastkiem we wszechświecie, szacowanym na około siódmą pod względem całkowitej obfitości w naszej galaktyce i Układzie Słonecznym. Uważa się, że jego występowanie jest w całości spowodowane syntezą przez fuzję węgla i wodoru w supernowych. Ze względu na zmienność pierwiastkowego azotu i jego związków z wodorem i tlenem, azot jest znacznie rzadszy na skalistych planetach wewnętrznego układu słonecznego i jest stosunkowo rzadkim pierwiastkiem na Ziemi. Jednak, podobnie jak na Ziemi, azot i jego związki występują powszechnie jako gazy w atmosferach planet i księżyców.,
azot w układach żywych
azot występuje we wszystkich organizmach żywych, głównie w aminokwasach tworzących białka oraz kwasach nukleinowych (DNA i RNA). Ciało ludzkie to około trzech procent azotu wagowo, czwarty co do wielkości pierwiastek po tlen, węgiel i wodór. Azot znajduje się w strukturze chemicznej prawie wszystkich neuroprzekaźników i jest definiującym składnikiem alkaloidów, cząsteczek biologicznych wytwarzanych jako metabolity wtórne przez wiele organizmów.,
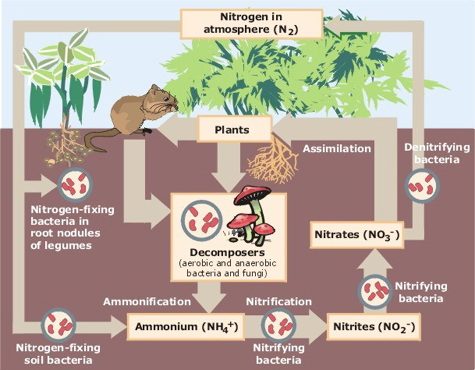
cykl azotowy opisuje ruch pierwiastka z powietrza do biosfery i związków organicznych oraz z powrotem do atmosfery. Syntetycznie wytwarzane azotany są kluczowymi składnikami nawozów przemysłowych i kluczowymi zanieczyszczeniami powodującymi eutrofizację systemów wodnych.
przemysłowa produkcja azotu
Gaz azotowy jest gazem przemysłowym wytwarzanym przez frakcyjną destylację ciekłego powietrza lub mechanicznie przy użyciu powietrza gazowego (tj. membrana odwróconej osmozy pod ciśnieniem lub adsorpcja zmiennociśnieniowa). Azot handlowy jest często produktem ubocznym przetwarzania powietrza w celu przemysłowego zagęszczania tlenu do produkcji stali i innych celów. Dostarczany sprężony w butlach jest często nazywany OFN (azot beztlenowy).,
w laboratorium chemicznym przygotowuje się go przez obróbkę wodnego roztworu chlorku amonu azotynem sodu lub przez rozkład azydku sodu:
NH_4Cl (AQ) + NaNO_2 (AQ) \rightarrow N_2 (g) + NaCl (Aq) + 2 H_2o (l)2 NaN_3 \rightarrow 2 na + 3 n_2
azot jest substancją chemiczną o właściwościach niemetalowy o elektroujemności 3,04. Ma pięć elektronów w swojej zewnętrznej powłoce i dlatego jest trójwalentny w większości związków. Wiązanie potrójne w cząsteczkowym azocie (N2)jest jednym z najsilniejszych znanych., Wynikająca z tego trudność przekształcania N2 w inne związki oraz łatwość (i związane z tym wysokie uwalnianie energii) przekształcania związków azotu w pierwiastek N2 zdominowały rolę azotu zarówno w przyrodzie, jak i w działalności gospodarczej człowieka.
widmo emisji azotu
azot cząsteczkowy (14n2) jest w dużej mierze przezroczysty dla promieniowania podczerwonego i widzialnego, ponieważ jest cząsteczką homonuklearną, a zatem nie ma momentu dipolowego, aby połączyć promieniowanie elektromagnetyczne w tych długościach fal., Znaczna absorpcja zachodzi przy ekstremalnych długościach fal ultrafioletowych, zaczynając od długości fali około 100 nanometrów. Wiąże się to z przemianami elektronowymi w cząsteczce do stanów, w których ładunek nie jest równomiernie rozłożony między atomami azotu. Absorpcja azotu prowadzi do znacznej absorpcji promieniowania ultrafioletowego w górnej atmosferze Ziemi i atmosferach innych ciał planetarnych.

azot jest stosowany również w przygotowywaniu próbek do analizy chemicznej w celu zagęszczenia i zmniejszenia objętości próbek ciekłych., Kierowanie strumienia azotu pod ciśnieniem prostopadle do powierzchni cieczy pozwala rozpuszczalnikowi odparować, pozostawiając rozpuszczony (- E) i nieuszkodzony rozpuszczalnik za sobą. Zbiorniki z azotem zastępują również dwutlenek węgla jako główne źródło zasilania pistoletów paintballowych. Ale azot musi być utrzymywany pod wyższym ciśnieniem niż CO2, dzięki czemu zbiorniki N2 są cięższe i droższe.
Dodaj komentarz