13 Anual de produtos Farmacêuticos Relatório
confira os outros artigos de destaque na edição deste mês:
Esteróides Wars: Novas Drogas Desafio Velhos Hábitos
a Modificação de Seu Regime de Glaucoma: Quando, Por que e Como
Faça o & Não fazer de Medicação Oral (CE)
Para pacientes com olho seco doença (DED), as opções de tratamento eram confinados em lágrimas artificiais, compressas quentes e ocasionais off-label esteróides., Enquanto alguns destes ajudam a acalmar os sintomas, eles fazem pouco para realmente controlar a doença, especialmente à medida que ela piora. Para os pacientes que já não podem ser tratados com esses remédios em casa, novas pesquisas mostram uma cascata de descobertas tanto no diagnóstico quanto no tratamento.
hoje em dia, os optometristas podem tratar estes doentes com medicamentos anti-inflamatórios orais e tópicos prescritos, tratamentos de ponto de atendimento, aquecimento e expressão de glândulas e até Opções avançadas, tais como membranas amnióticas. Enquanto estes avanços estão dando aos nossos pacientes uma nova Locação no conforto ocular, optometristas têm muito mais para navegar., A aplicação do tratamento mais apropriado ainda varia muito dentro das práticas optométricas.3
embora não exista um consenso claro sobre a prescrição de medicamentos para os olhos secos, compreender como estes medicamentos funcionam pode ajudar os médicos a adaptar a gestão eficaz para cada paciente.
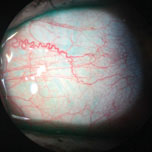
os vasos sanguíneos inflamados deste doente podem ser vistos sem quaisquer corantes vitais. Foto: Vin Dang, OD. Clique na imagem para ampliar.,
A Perda da Homeostase
Quando se trata de tratamento de DED pacientes, oportuna e eficaz opções podem ser complicada pela necessidade de detectar com precisão e identificar etiologias subjacentes. Em 2017, A Tear Film and Ocular Surface Society (TFOS) lançou uma nova luz sobre a DED com o seu segundo relatório da Dry Eye Workshop (DEWS II). Essa pesquisa refuta DED como uma condição multifactorial caracterizada por uma perda de homeostase do filme lacrimogêneo e acompanhada por sintomas oculares que levam à instabilidade do filme lacrimogêneo e hiperosmolaridade.,1 This turned on its head the old paradigm of categorizing DED as EAS Wear aqueous-defficient dry eye (ADDE) or evaporative dry EES (EDE). Com as conclusões do DEWS II, estas já não são consideradas condições de superfície ocular completamente separadas, já que pesquisadores descobriram que até 70% dos pacientes com DDE possuem etiologias mistas.2 na vanguarda dessa perda de homeostase está a inflamação.,
O Relatório TFOS DEWS II também nos ensinou que ” na DED, a hiperosmolaridade lacrimogénea é considerada a criação de uma cascata de eventos sinalizadores dentro das células epiteliais superficiais, que leva à libertação de mediadores inflamatórios e proteases. Tais mediadores, juntamente com a hiperosmolaridade lacrimogénea em si, são concebidos para causar a perda de células epiteliais e epiteliais e danos ao glicocalyx epitelial. A lesão é reforçada por mediadores inflamatórios das células T activadas, recrutados para a superfície ocular., O resultado final é a característica pontuada epiteliopatia de DED e uma instabilidade de filme lacrimogêneo que leva em algum ponto à ruptura inicial do filme lacrimogêneo. Esta separação agrava e amplifica a hiperosmolaridade lacrimogénea e completa o círculo vicioso de eventos que levam a danos na superfície ocular.”1 este círculo vicioso inflamatório é um caminho comum em que todas as formas de DED entram, independentemente da etiologia.
inflamação
na superfície ocular, a fase aguda da inflamação resulta na degranulação de mastócitos e na subsequente libertação de histamina e fosfolípidos., Os estímulos inflamatórios também iniciam a degradação da membrana celular através da fosfolipase A2 e, subsequentemente, levam à formação de ácido araquidónico (AA). Este último é metabolizado por isoenzimas 5-lipoxigenase (LOX) e ciclo-oxigenase (COX-1/COX-2), resultando no recrutamento de glóbulos brancos e na formação de prostaglandinas e tromboxano A2, respectivamente.4,5 prostaglandinas desempenham um papel na resposta à dor e aumentam a permeabilidade dos vasos.,
Um dos muitos impactos desta cascata é a produção e liberação de citocinas inflamatórias, como interleucina-1 (IL-1), fator de necrose tumoral-alfa (TNF-a), interleucina-6 (IL-6) e metaloproteinases de matriz (MMPs) pela superfície ocular células epiteliais.1,5 isto resulta na activação de células que apresentam antigénios e no aumento da expressão de moléculas de adesão, tais como a molécula-1 (ICAM-1) de adesão intercelular e as selectinas pelo endotélio vascular conjuntival.5 isto facilita o recrutamento de células inflamatórias adicionais para a superfície ocular., a inflamação crónica envolve o processamento de antigénios por células que apresentam antigénios oculares e por células T ingénuas. As células T primadas do CD-4 aderem ao endotélio vascular activado e entrarem no tecido ocular. As citoquinas produzidas por células T activadas, tais como o interferão gama (IFN-Y), amplificam a resposta imunitária através do aumento da expressão da molécula de adesão por vasos sanguíneos oculares.Os metabolitos do ácido araquidónico, tais como os leucotrienos e as prostaglandinas, estão activamente envolvidos no desenvolvimento da doença inflamatória.,4 reconhecer a importância e complexidade da inflamação na DED dá-nos a oportunidade de identificar lacunas ou sobreposições no tratamento, desde que possamos identificar onde cada prescrição se encaixa ao longo da cascata.
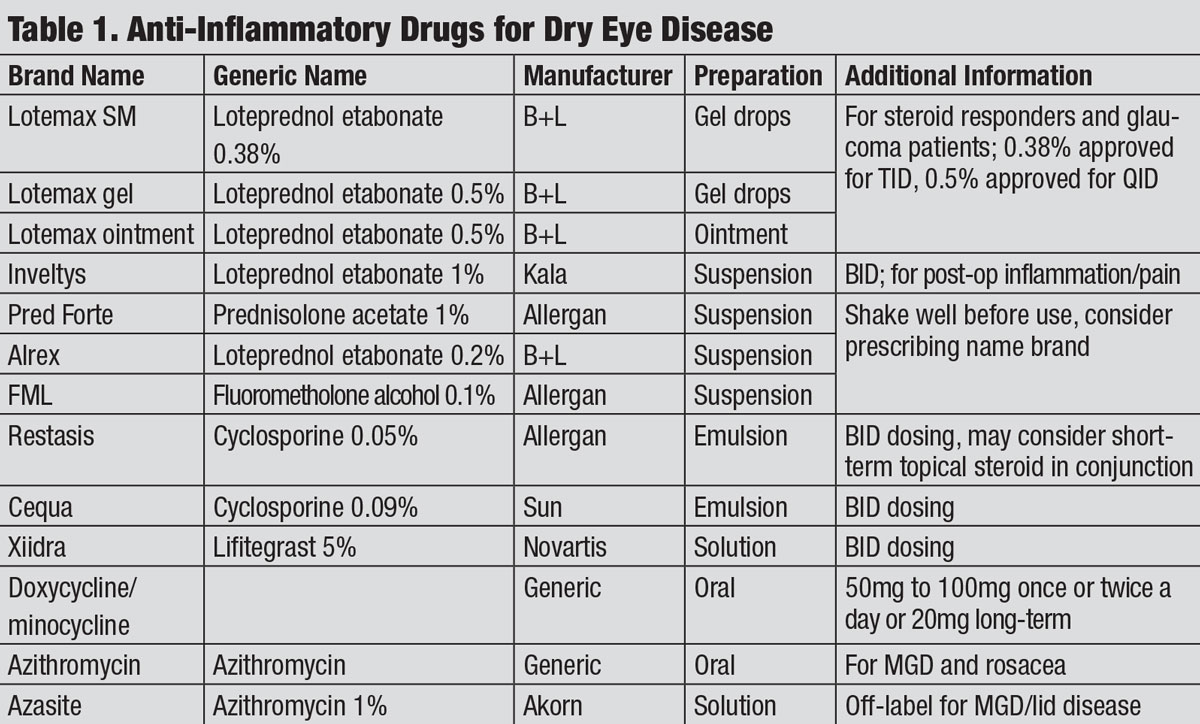
anti-inflamatórios para a doença do olho seco. Clique na mesa para ampliar. estes medicamentos tópicos estimulam a produção de uma glicoproteína chamada lipocortina., A lipocortina formada inibe a actividade da fosfolipase A2, que liberta ácido araquidónico e, em última análise, resulta na formação de prostaglandinas e esteróides tromboxano A2.6 também inibem a formação de IL-1, ICAM-1, MMPs e citoquinas.Estas acções produzem efeitos anti-inflamatórios e imunossupressores num nível localizado à medida que os esteróides bloqueiam as vias LOX e COX-1/COX-2 da cascata inflamatória, reduzindo a vasodilatação, permeabilidade vascular e estabilizando as membranas celulares.,7 Os ensaios clínicos de
mostram melhorias significativas nos doentes com ADDE moderada a grave, com melhorias na coloração da córnea e injecção geral.Como resultado, estes medicamentos são muitas vezes altamente eficazes opções anti-inflamatórias de curto prazo para pacientes com inflamação da superfície ocular. a escolha do corticosteróide mais adequado para o seu doente requer conhecimento tanto do mecanismo de Acção do medicamento como do seu doente em particular., Do ponto de vista clínico, o loteprednol tem inúmeras indicações oftálmicas e também vem em uma ampla variedade de formulações, tornando-se uma opção flexível para os praticantes.8
novas versões da distribuição tópica de drogas para loteprednol também contribui para o recurso. Lotemax SM gel (loteprednol 0, 38%, Bausch + Lomb) usa partículas submicron para aumentar a dissolução do fármaco nas lágrimas, o que aumenta a penetração transcorneal em comparação com o Lotemax 0, 5% gel gotas e permite uma maior adesão à superfície ocular.,Além disso, o Lotemax SM é também preservado com uma dose baixa de cloreto de benzalcónio (BAK) e com uma dosagem TID, reduzindo a carga numa superfície ocular já comprometida. Por esta mesma razão, além de menos efeitos secundários indesejáveis (Cataratas subapsulares e foi elevada), o Lotemax SM é um bom anti-inflamatório de curto prazo para pacientes que sofrem de DED concomitante e glaucoma.
embora não tenha sido aprovado pela FDA para a gestão da DED, tem sido usado como um tratamento off-label para muitos pacientes de olho seco com base no consenso da literatura profissional revisada por pares.,
outra opção do loteprednol é o Inoveltys (suspensão de etabonato de loteprednol a 1%, Kala), que liga o loteprednol a uma nanopartícula que penetra muco para melhorar a penetração e a concentração do fármaco no tecido ocular.10 por último, embora ainda não aprovado pela FDA, é outra opção loteprednol, KPI-121 0.25% (suspensão etabonato de loteprednol 0.25%, Kala), que seria especificamente aprovado para sinais e sintomas de DED.Fora do loteprednol, existem muitas opções alternativas para o tratamento da inflamação da superfície ocular, incluindo FML (suspensão oftálmica fluorometolona 0.,25%, 0, 1%, Alergano) ou acetato de prednisolona 0, 12%. Estes estão disponíveis em formulações genéricas e podem ser eficazes na gestão DED, especialmente porque custam menos do que os homólogos de marca.
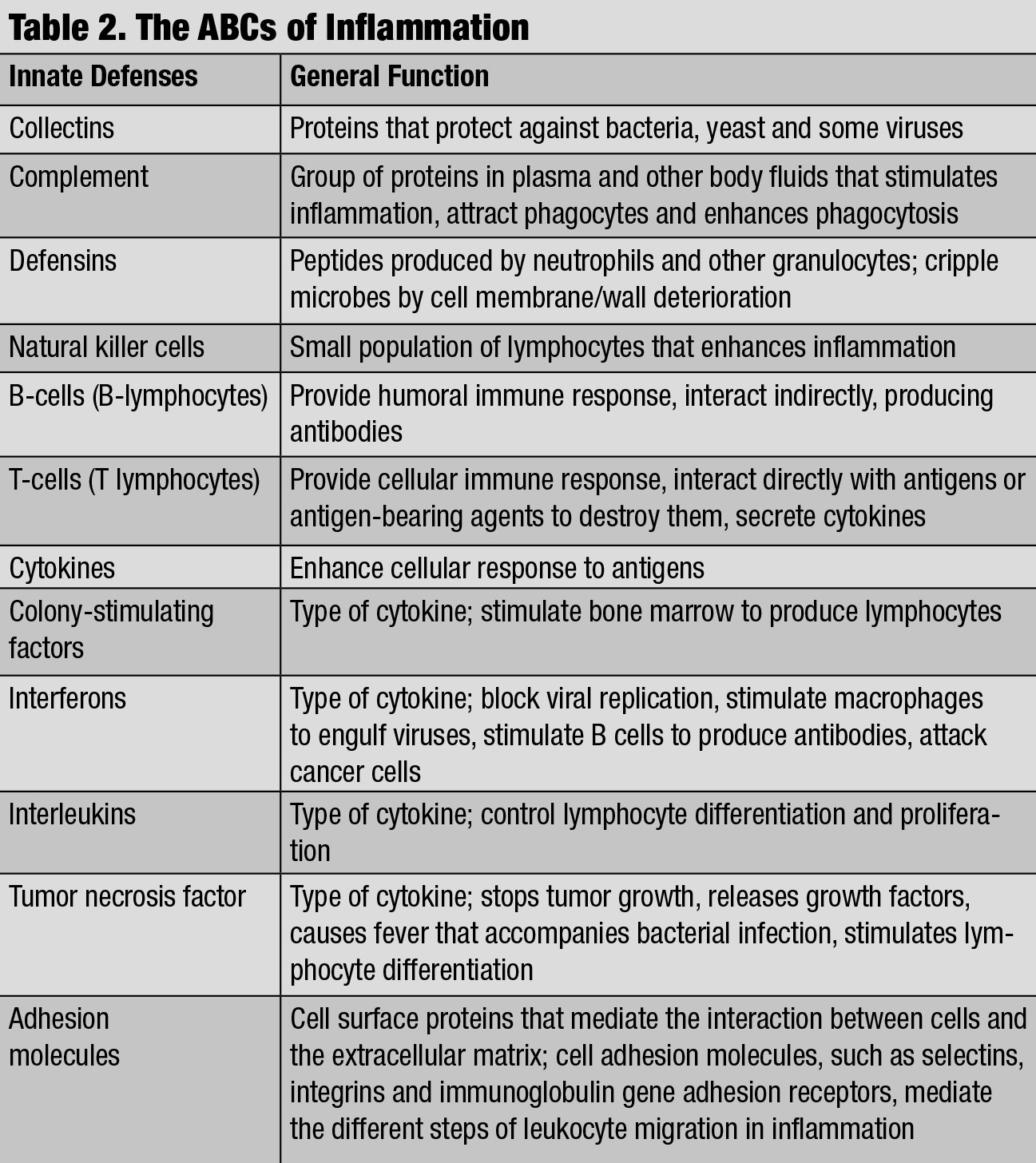
The ABCs of Inflammation. Clique na mesa para ampliar.
imunomoduladores de ciclosporina
Restasis (ciclosporina a emulsão a 0, 05%, Alergano) é um imunomodulador que actua sobre as células T na película lacrimogénea, conjuntiva e córnea, e está disponível para uso oftálmico desde 2003.,A ciclosporina a (CsA) suprime a inflamação ligando-se à proteína ciclofilina, o que resulta na redução da formulação interleucina-2 (IL-2) e na supressão da activação das células T. o lL-2 é secretado pelas células T-helper e estimula a proliferação de células T citotóxicas e células T-helper adicionais.12, 13
Como o CsA interrompe a activação das células-T, mas não visa as células-T já activas, pode não haver uma melhoria imediata nos sinais DED. Por esta razão, os médicos geralmente prescrevem uma dose curta de corticosteróides após o início da Restase., Uma fonte adicional de descumprimento do paciente surge do veículo de entrega de drogas. CsA 0, 05% requer suspensão em um agente emulsionante, como glicerina ou óleo de rícino, uma vez que tem uma fraca solubilidade em água por si só. Esta suspensão contribui para alguns dos efeitos secundários, tais como ardor picante e hiperemia.13
Cequa (ciclosporina 0, 09% solução oftálmica, oftalmia solar) foi aprovado pela FDA em 2018 e entrou recentemente no mercado oftálmico.14 Administração de doses com tecnologia nanomicelar (Ncell, oftalmia solar) para evitar os problemas de solubilidade com CsA 0.,05%, a Cequa tem como objetivo proporcionar à Olho a maior concentração de CsA no mercado.14 Nanomicelas possuem propriedades hidrofílicas e hidrofóbicas, o que aumenta sua capacidade de penetrar efetivamente o epitélio ocular com irritação mínima ou degradação de drogas.Com um perfil de efeito secundário semelhante à Restase, terá de ser visto como a conformidade do doente responde ao nível de concentração mais elevado da ciclosporina e se o uso concomitante de esteróides será necessário para o alívio eficaz dos sintomas.,
outros imunomoduladores
Xiidra (solução oftálmica lifitegrast 5%, Novartis) entraram no mercado em 2016 e é actualmente o único tratamento aprovado para ambos os sinais e sintomas da DED.Semelhante à Ciclosporina, A Xiidra inibe também a via inflamatória mediada pelas células T, impedindo o recrutamento e a activação para a superfície ocular. No entanto, Xiidra actua bloqueando a interacção entre o antigénio 1 (LFA-1) associado à função linfocitária e a molécula de adesão intercelular 1 (ICAM-1).,O bloqueio desta interacção das células T LFA-1on e ICAM-1 reduz a activação e migração das células T do vaso sanguíneo para a superfície ocular, bem como a secreção de citoquinas pró-inflamatórias múltiplas (por exemplo, IL-1, TNF-a, IFN-Y), reduzindo a inflamação.Ensaios clínicos com lifitegrast demonstraram melhoria estatisticamente significativa nos sinais e sintomas da DD.Com a posologia sem conservantes, os efeitos secundários mais frequentes são queimadura, borrão na instilação e disgeusia., Do ponto de vista farmacológico, os mediadores inflamatórios ainda estão presentes na superfície ocular quando Xiidra é iniciado, e um esteróide ainda pode ser empregado para melhorar o conforto do paciente. Dito isto, muitos pacientes são tratados com sucesso com Xiidra como tratamento de primeira linha ou autônomo.
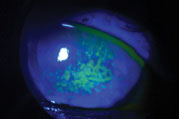
fluoresceína sódica coloração mostra que a superfície da córnea deste doente está comprometida por doença ocular seca. Foto: Vin Dang, OD. Clique na imagem para ampliar.
antibióticos
tetraciclina Oral e derivados das tetraciclinas (ex.,, doxiciclina, minociclina) pode ser usado para tratar doenças associadas ao DED, tais como rosácea, blefarite e disfunção da glândula meibomiana. Estes antibióticos de largo espectro regulam os lípidos e inibem a síntese proteica bacteriana, além de ter propriedades anti-inflamatórias.2 pesquisas mostram que eles podem diminuir a atividade de MMP e fosfolipase A2, bem como reduzir a produção de mediadores inflamatórios como IL-1 e TNF-a, resultando em irritação reduzida e maior estabilidade da película lacrimogénea.,2 estas características tornam – nos uma opção atraente para a gestão a curto prazo da inflamação ocular ou a longo prazo a uma dose mais baixa, com efeitos secundários mínimos.Outra opção de tratamento antibiótico é a azitromicina oral, uma vez que as propriedades anti-inflamatórias ajudam a controlar a inflamação da tampa, inibindo as citoquinas pró-inflamatórias e a flora bacteriana.Embora não exista um acordo universal sobre a dosagem, um tratamento mais curto, utilizando 250 mg a 500 mg ao longo de cinco dias, pode ser eficaz no tratamento da rosácea.,Quando se trata de tomar uma decisão de prescrição para um tratamento oral, considere a azitromicina como uma opção inicial, salvo contra-indicação em contrário. Um estudo publicado em 2019 demonstrou que a eficácia da azitromicina oral foi superior à doxiciclina oral para o tratamento da disfunção da glândula meibomiana quando se considera a dosagem e a duração.A Azasite (solução oftálmica de azitromicina a 1%, Akorn) foi aprovada pela FDA para a conjuntivite bacteriana, mas foi bem tolerada para o tratamento fora do rótulo da disfunção da glândula meibomiana e da EDE., Além da diminuição nos mediadores inflamatórios e supressão dos mediadores pró-inflamatórios, pesquisas mostram que a azitromicina tópica pode melhorar o comportamento lipídico das secreções da glândula meibomiana.Nenhuma pesquisa ainda mostra qualquer benefício para a combinação de antibióticos sistêmicos e tópicos para melhorar o tratamento DED. como pesquisas recentes mostram, o DED é complexo e desafiador. Antes que os ODs possam começar a geri-lo, eles requerem uma compreensão diagnóstica clara da superfície ocular de cada paciente., Isto significa identificar quaisquer condições oculares concomitantes, bem como factores sistémicos que possam exacerbar a doença. ao determinar o tratamento, os clínicos devem considerar a osmolaridade, a inflamação, a história do tratamento e a coloração da superfície ocular. Dito isto, utilizando estes indicadores, os optometristas devem prescrever uma terapêutica ocular seca que inclua alvos específicos ao longo da cascata inflamatória, especialmente no início da apresentação da doença. Além disso, abordar o tratamento e a gestão com flexibilidade pode servir estes pacientes mais a longo prazo., Apesar de opções fora do rótulo, considere a administração de tid ou QID CsA, prescrevendo tratamentos anti-inflamatórios concomitantes, tais como Restasis e Xiidra, ou um tratamento CsA juntamente com antibióticos orais para tratar e controlar eficazmente os sinais e sintomas do doente. O uso de múltiplas terapias e modalidades para abordar os sintomas no início pode proporcionar essa vantagem adicional. em última análise, é essencial educar os doentes e enfatizar a importância da gestão ao longo da vida para a DED., Haverá dias bons e dias maus, bem como melhores e piores épocas do DED, e as modificações de gestão nem sempre são contratempos no curso da doença.o Dr. Grant é instrutor clínico no Southern College of Optometry em Memphis, Tenn.
Deixe uma resposta