inlärningsmål
- diskutera kväveens egenskaper.
nyckelpunkter
- kväve är ett kemiskt element med symbol N och atomnummer 7. Elementärt kväve är en färglös, luktfri, smaklös och mestadels inert diatomisk gas vid standardförhållanden, som utgör 78.09 procent av jordens atmosfär i volym.,
- kvävegas är en industrigas som produceras genom fraktionerad destillation av flytande luft eller på mekanisk väg med hjälp av gasformig luft. Kommersiellt kväve är ofta en biprodukt av luftbearbetning för industriell koncentration av syre.
- kvävegas har en mängd olika tillämpningar, inklusive att fungera som en inert ersättning för luft där oxidation är oönskad. Flytande kväve används också för att kryogeniskt frysa föremål.
villkor
- elementalOf, som hänför sig till, eller är ett element (i motsats till en förening).,
- aminosyraallmänt, molekyler som innehåller både en amino och en karboxylsyrafunktionell grupp. Monomererna från vilka polypeptidkedjor eller proteiner byggs är aminosyror.
- nitrogenA kemiska element (symbol N) med atomnummer av 7 och atomvikt 14.0067 amu.
elementet kväve upptäcktes som en separerbar del av luft av skotska läkaren Daniel Rutherford 1772. Kväveföreningar var välkända under medeltiden. Alkemister visste salpetersyra som aqua fortis (starkt vatten)., Blandningen av salpetersyra och saltsyra var känd som aqua regia (kungligt vatten), firade för sin förmåga att lösa upp guld (kungen av metaller). De tidigaste militära, industriella och jordbruksapplikationer av kväveföreningar använde saltpeter (natriumnitrat eller kaliumnitrat), framför allt i krut och senare som gödningsmedel.
kväve är ett kemiskt element med symbol N och atomnummer 7. Elementärt kväve är en färglös, luktfri, smaklös och mestadels inert diatomisk gas vid standardförhållanden, som utgör 78.09 procent av jordens atmosfär i volym., Kväve är ett vanligt element i universum, uppskattat till ungefär sjunde i total överflöd i vår galax och solsystemet. Dess förekomst tros vara helt på grund av syntes genom fusion av kol och väte i supernovor. På grund av volatiliteten hos elementärt kväve och dess föreningar med väte och syre är kväve mycket mindre vanligt på de steniga planeterna i det inre solsystemet och är ett relativt sällsynt element på jorden. Men som på jorden, kväve och dess föreningar förekommer vanligen som gaser i atmosfären av planeter och månar.,
kväve i levande system
kväve förekommer i alla levande organismer, främst i aminosyror som utgör proteiner och nukleinsyror (DNA och RNA). Människokroppen är ungefär tre procent kväve i vikt, det fjärde mest rikliga elementet efter syre, kol och väte. Kväve finns i den kemiska strukturen hos nästan alla neurotransmittorer och är en definierande komponent i alkaloider, biologiska molekyler som produceras som sekundära metaboliter av många organismer.,
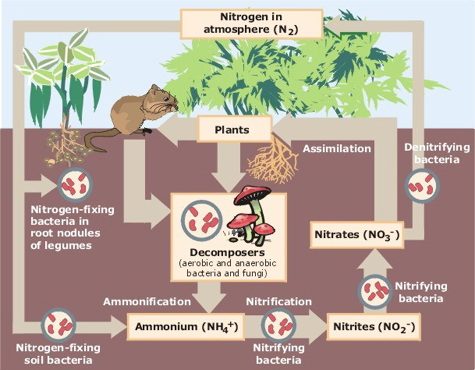
kvävecykeln beskriver elementets rörelse från luften till biosfären och organiska föreningar och tillbaka in i atmosfären. Syntetiskt producerade nitrater är viktiga ingredienser i industriella gödningsmedel och viktiga föroreningar som orsakar eutrofiering av vattensystem.
industriell produktion av kväve
kvävegas är en industriell gas som produceras genom fraktionerad destillation av flytande luft eller på mekanisk väg med hjälp av gasformig luft (dvs trycksatt omvänd osmos membran eller tryck swing adsorption). Kommersiell kväve är ofta en biprodukt av luftbearbetning för industriell koncentration av syre för ståltillverkning och andra ändamål. När den levereras komprimerad i cylindrar kallas den ofta OFN (syrefritt kväve).,
i ett kemiskt laboratorium framställs det genom behandling av en vattenhaltig lösning av ammoniumklorid med natriumnitrit, eller genom sönderdelning av natriumazid:
Nh_4cl (aq) + NaNO_2 (aq) \rightarrow N_2 (g) + NaCl (aq) + 2 H_2O (L)2 NaN_3 \rightarrow 2 Na + 3 N_2
kemiska egenskaper hos kväve
kväve är en nonmetal med en elektronegativitet på 3,04. Den har fem elektroner i sitt yttre skal och är därför trivalent i de flesta föreningar. Trippelbindningen i molekylärt kväve (N2) är en av de starkaste kända., Svårigheten att omvandla N2 till andra föreningar, och den lätthet (och tillhörande högenergifrisättning) att omvandla kväveföreningar till elementärt N2, har dominerat kväveens roll både i naturen och i den mänskliga ekonomiska verksamheten.
Kväveutsläppsspektrum
molekylärt kväve (14N2) är i stor utsträckning transparent för infraröd och synlig strålning eftersom det är en homonukleär molekyl och har därför inget dipolmoment för att koppla ihop den elektromagnetiska strålningen vid dessa våglängder., Signifikant absorption sker vid extrema ultravioletta våglängder, som börjar vid en våglängd på cirka 100 nanometer. Detta är förknippat med elektroniska övergångar i molekylen till tillstånd där laddningen inte fördelas jämnt mellan kväveatomer. Kväveabsorption leder till signifikant absorption av ultraviolett strålning i jordens övre atmosfär och atmosfärerna hos andra planetariska kroppar.

kväve används också i förbereda prover för kemisk analys för att koncentrera och minska volymen av flytande prover., Genom att rikta en trycksatt ström av kvävegas vinkelrätt mot vätskans yta kan lösningsmedlet förångas samtidigt som lösningsmedlet(lösningarna) och det ojämna lösningsmedlet lämnas bakom. Kväve tankar ersätter också koldioxid som huvudkraftkälla för paintball gevär. Men kväve måste hållas vid högre tryck än CO2, vilket gör N2-tankar tyngre och dyrare.
Lämna ett svar