Tudomány > Kémia > Megoldások, illetve A Colligative Tulajdonságok > Rövid Kiszámítására szolgáló Módszereket, Koncentráció, az Oldatok
ebben A cikkben, meg kell tanulni rövid módszerek kiszámításához molality, molarity, stb.
ezek a módszerek csak versenyvizsgákon használhatók.,
a Közvetlen Képlet Kiszámításához Molality, valamint Molarity:

Ahol M = molarity a mol L-1 vagy M
m = molality a mol kg-1 vagy m
a = % által tömege mennyiségével
d = sűrűség megoldás, g/mL vagy g cm-3.,
MB = Molekuláris tömege mennyiségével gramm
MA = Molekuláris tömege oldószer gramm
Megjegyzés: Ha használja ezeket a képleteket, vigyázzon, hogy a mennyiség az előírt egységek
Molekuláris tömegek bizonyos anyagok gramm:
Numerikus Problémák Kiszámításához Molality, valamint Molarity:
Példa – 01:
A sűrűsége megoldást tartalmazó 13 tömeg % – os kénsavat, az 1.09 g/mL. Számítsa ki az oldat molaritását és normalitását
adott: a = 13, d = 1,09 g / mL
A találáshoz: Molaritás (M) =? és normalitás (N)=?,
Megoldás:
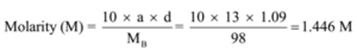
n = Molekuláris tömeg/egyenértékű tömeg = 98 g/49 g = 2
a Normalitás = molarity x n = 1.446 x 2 = 2.892 N
Példa – 02:
A sűrűsége 2.03 M ecetsav oldat (molekuláris tömege = 60) a víz 1.017 g/mL. Számítsa ki az oldat molalitását
adott: M = 2,03, MB = 60 g mol-1, d = 1,017 g / mL
hogy megtalálja: Molality (m) = ?,
megoldás:

molality = m = 1/0.4410 = 2,268 molal
példa – 03:
a KCL oldat tömegének 10,0% – os sűrűsége vízben 1,06 g/ml. Számítsa ki a KCL molalitását, molaritását és mólfrakcióját.
adott: a = 10, d = 1,06 g / mL
megtalálni: Molaritás (M) =?, molalitás (m)=?, mole fraction (XB) =?
megoldás:

Ans: Molarity 1.,42 M, Molality = 1.491 m, Mole fraction = 0.0261
Example – 04:
0.8 M solution of H2SO4 has a density of 1.06 g/cm3. calculate molality and mole fraction
Given: M = 0.8 M, d = 1.06 g/cm3.
To Find: Molality (m) =?, mole fraction (XB) =?
Solution:

molality = m = 1/1.227 = 0.814 molal

0.814 x 18 x (1 – XB) = 1000 XB
14.,652 – 14.652 XB = 1000 XB
1014.652 XB = 14.652
XB = 14.652/1014.652 = 0.014
példa-05:
egy 6.90 M KOH vízben lévő oldat 30 tömegszázalék KOH-t tartalmaz. Számítsa ki az oldat sűrűségét.
adott: M = 6,90 M, a = 30
megtalálni: az oldat sűrűsége = d = ?
megoldás:

Ans: az oldat sűrűsége = 1,288 g/mL
példa – 06:
adott: a = 10, D = 1.070 g cm-3,
megtalálni: Mole frakció =? molarity = ?, and molality =?
Solution:

Example – 07:
Calculate the mole fraction of solute in its 2 molal aqueous solution.
Given: molality = 2 molal
To Find: Mole fraction =?,
Solution:

Previous Topic: Numerical Problems on Molality
Next Topic: Solutions of Gases in Liquids
Vélemény, hozzászólás?