Vitenskap > Kjemi > Løsninger og Deres Colligative Egenskaper > Kort-cut Metoder For å Beregne Konsentrasjonen av Løsninger
I denne artikkel, vi skal studere short-cut metoder for å beregne molality, molarity, etc.
Disse metodene kan bare brukes i konkurranseutsatte eksamen bare.,
Direkte Formler for å Beregne Molality og Molarity:

Hvor M = molarity i mol L-1 eller M –
m = molality i mol kg-1 eller m –
a = % av massen av oppløst stoff
d = tetthet av løsning i g/mL eller g cm-3.,
MB = Molekylære massen av oppløst stoff i gram
MA = Molekylær masse i gram løsemiddel
Merk: Når du bruker disse formler, ta vare på at mengder er i foreskrevet enheter
Molekylær masser av visse stoffer i gram:
Numeriske Problemer med å Beregne Molality og Molarity:
Eksempel – 01:
tettheten av en løsning som inneholder 13 % av massen av svovelsyre er 1,09 g/mL. Beregne molarity og normalitet av løsningen
Gitt: a = 13, d = 1.09 g/mL
for Å Finne: Molarity (M) =? og Normalitet (N) =?,
Løsning:
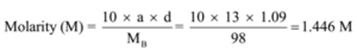
n = Molekylær masse/tilsvarende masse = 98 g/49 g = 2
Normalitet = molarity x n = 1.446 x 2 = 2.892 N
Eksempel – 02:
tettheten av 2.03 M løsning av eddiksyre (molekylær masse = 60) i vann er 1.017 g/mL. Beregne molality av løsningen
Gitt: M = 2.03, MB = 60 g mol-1, d = 1.017 g/mL
for Å Finne: Molality (m) = ?,
Løsning:

molality = m = 1/0.4410 = 2.268 molal
Eksempel – 03:
tettheten av 10.0% av massen av KCl løsning i vann er 1.06 g/mL. Beregne molality, molarity og mole brøkdel av KCl.
Gitt: a = 10, a = 1.06 g/mL
for Å Finne: Molarity (M) =?, molality (m) =?, mole brøkdel (XB) =?
Løsning:

Ans: Molarity 1.,42 M, Molality = 1.491 m, Mole fraction = 0.0261
Example – 04:
0.8 M solution of H2SO4 has a density of 1.06 g/cm3. calculate molality and mole fraction
Given: M = 0.8 M, d = 1.06 g/cm3.
To Find: Molality (m) =?, mole fraction (XB) =?
Solution:

molality = m = 1/1.227 = 0.814 molal

0.814 x 18 x (1 – XB) = 1000 XB
14.,652 – 14.652 XB = 1000 XB
1014.652 XB = 14.652
XB = 14.652/1014.652 = 0.014
Eksempel – 05:
En 6.90 M løsning av KOH i vann inneholder 30% av massen av KOH. Beregne tettheten av løsning.
Gitt: M = 6.90 M, a = 30
for Å Finne: tetthet av løsning = d = ?
Løsning:

Ans: Tetthet av løsning = 1.288 g/mL
Eksempel – 06:
Gitt: a = 10, a = 1.070 g cm-3,
for Å Finne: mole brøkdel =? molarity = ?, and molality =?
Solution:

Example – 07:
Calculate the mole fraction of solute in its 2 molal aqueous solution.
Given: molality = 2 molal
To Find: Mole fraction =?,
Solution:

Previous Topic: Numerical Problems on Molality
Next Topic: Solutions of Gases in Liquids
Legg igjen en kommentar