Was ist Homöopathie?
Homöopathie ist eine alternative medizinische Praxis, die in den späten 1700er Jahren entwickelt wurde. Homöopathie basiert im Allgemeinen auf zwei Hauptprinzipien:
- dass eine Substanz, die Symptome bei einem gesunden Menschen verursacht, in verdünnter Form zur Behandlung von Symptomen und Krankheiten verwendet werden kann, ein Prinzip, das als „like-cures-like“ bekannt ist; und
- je verdünnter die Substanz ist, desto potenter ist sie, was als „Gesetz der Unendlichkeiten“ bekannt ist.,“
Historisch gesehen wurden homöopathische Produkte durch „Beweise“ identifiziert, bei denen gesunden Freiwilligen Substanzen in Konzentrationen verabreicht werden, die Symptome verursachen. Symptome von Freiwilligen werden aufgezeichnet, um mögliche therapeutische Anwendungen für die Substanzen anzuzeigen. Mit anderen Worten, wenn eine Substanz ein bestimmtes Symptom verursacht, würden Personen, bei denen dieses Symptom auftritt, mit einer verdünnten Lösung aus dieser Substanz behandelt.
Was sind homöopathische Produkte und wie können Sie feststellen, dass Sie eines einnehmen?,
Es gibt keine von der FDA zugelassenen Produkte, die als homöopathisch gekennzeichnet sind; Dies bedeutet, dass jedes als homöopathisch gekennzeichnete Produkt in den USA ohne FDA-Bewertung auf Sicherheit oder Wirksamkeit vermarktet wird. Diese Produkte werden häufig als natürliche, sichere und wirksame Alternativen zu zugelassenen verschreibungspflichtigen und nicht verschreibungspflichtigen Produkten vermarktet und online und in großen Einzelhandelsgeschäften verkauft.
Produkte, die als homöopathisch gekennzeichnet sind, können eine breite Palette von Substanzen enthalten, einschließlich Inhaltsstoffen aus Pflanzen, gesunden oder erkrankten tierischen oder menschlichen Quellen, Mineralien und Chemikalien.,
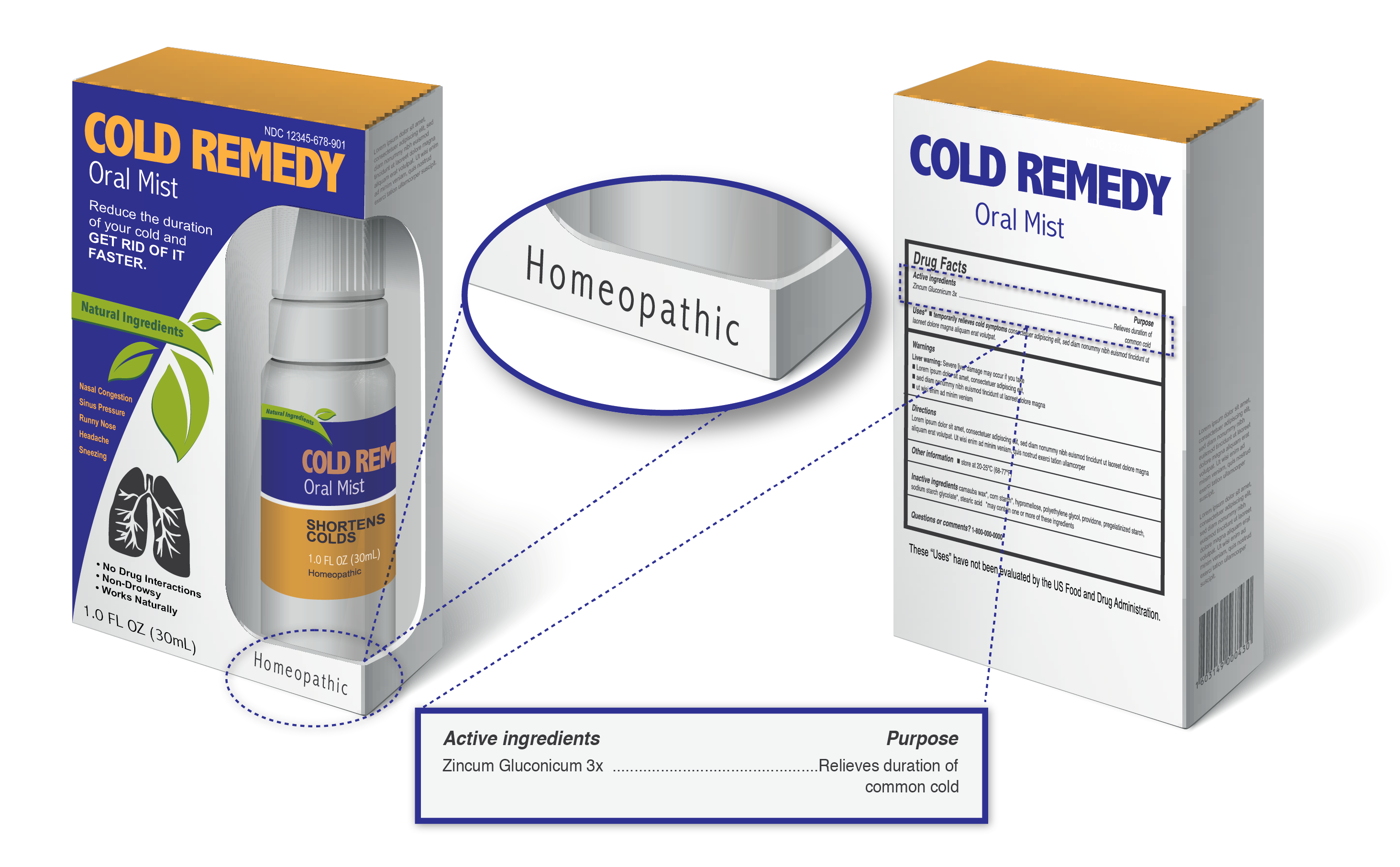
Produkte, die als homöopathisch gekennzeichnet sind, umfassen im Allgemeinen:
- Das Wort „Homöopathisch“
- Die in Bezug auf die Verdünnung aufgeführten Inhaltsstoffe, z. B. 1X, 6X, 2C
Zurück nach oben
Ist die FDA besorgt über die Sicherheit homöopathischer Produkte?
Während Produkte, die als homöopathisch gekennzeichnet sind, im Allgemeinen als stark verdünnt gekennzeichnet sind, wurde festgestellt, dass einige dieser Produkte messbare Mengen an Wirkstoffen enthalten und daher erhebliche Patientenschäden verursachen können., Darüber hinaus hat die FDA Produkte getestet, die nicht ordnungsgemäß hergestellt wurden, was zu falschen Verdünnungen führen und das Kontaminationspotenzial erhöhen kann. Darüber hinaus werden einige als homöopathisch gekennzeichnete Produkte zur Behandlung schwerer Krankheiten oder Erkrankungen vermarktet.,nweiter Rückruf von homöopathischen Arzneimitteln auf Wasserbasis aufgrund mikrobieller Kontamination
Was sollten Verbraucher über homöopathische Produkte wissen?,
Produkte, die als homöopathisch gekennzeichnet und derzeit in den USA vermarktet werden, wurden von der FDA nicht auf Sicherheit und Wirksamkeit zur Diagnose, Behandlung, Heilung, Vorbeugung oder Milderung von Krankheiten oder Zuständen überprüft. Die evidenzbasierten Arzneimittelprüfungen der FDA spielen eine wesentliche Rolle bei der Gewährleistung, dass Arzneimittel mit hochwertigen Herstellungsprozessen hergestellt werden und für die beabsichtigte Verwendung sicher und wirksam sind., Produkte, die nicht auf Sicherheit und Wirksamkeit geprüft wurden, können Verbrauchern, die sich für die Behandlung schwerer Krankheiten oder Erkrankungen mit solchen Produkten entscheiden, schaden, und Verbraucher können auf die Behandlung mit einem Medizinprodukt verzichten, das wissenschaftlich als sicher und wirksam erwiesen wurde.
FDA empfiehlt Verbrauchern, mit ihrem Arzt oder Arzt über sichere und wirksame Behandlungen für ihre Krankheit oder ihren Zustand zu sprechen.
Zurück nach oben
Wie werden homöopathische Produkte reguliert?,
Nach dem Bundesgesetz über Lebensmittel, Arzneimittel und Kosmetika unterliegen homöopathische Produkte den gleichen Anforderungen in Bezug auf Zulassung, Verfälschung und Markenmissbrauch wie andere Arzneimittel. Derzeit sind keine homöopathischen Produkte von der FDA zugelassen.
Im Jahr 1988 veröffentlichte die FDA den Compliance Policy Guide (CPG) 400.400 mit dem Titel „Bedingungen, unter denen homöopathische Arzneimittel vermarktet werden können“, in dem die Durchsetzungspolitik der Agentur beschrieben wurde. Oktober 2019 zog die FDA CPG 400.400 zurück, da dies nicht mit unserem risikobasierten Ansatz für Regulierungs-und Durchsetzungsmaßnahmen vereinbar ist., Die FDA gab auch einen überarbeiteten Entwurf einer Anleitung heraus: Arzneimittel, die als homöopathisch gekennzeichnet sind, für öffentliche Kommentare. Da homöopathische Arzneimittel von der FDA für keine Verwendung zugelassen wurden, entsprechen sie möglicherweise nicht den modernen Standards für Sicherheit, Wirksamkeit und Qualität.
Dieser überarbeitete Leitlinienentwurf schlägt einen umfassenden, risikobasierten Durchsetzungsansatz für homöopathische Produkte vor, die ohne FDA-Zulassung vermarktet werden.
Der von der FDA vorgeschlagene Ansatz priorisiert Regulierungs-und Durchsetzungsmaßnahmen mit nicht zugelassenen homöopathischen Produkten, die das größte Risiko für Patienten darstellen., Viele homöopathische Produkte werden wahrscheinlich außerhalb der risikobasierten Kategorien liegen, die im überarbeiteten Leitlinienentwurf beschrieben sind. Die FDA beabsichtigt, ihre Durchsetzungsbehörden auf die folgenden Arten von Produkten zu konzentrieren:
- mit gemeldeten Sicherheitsbedenken;
- , die Inhaltsstoffe enthalten oder vorgeben, die mit potenziell signifikanten Sicherheitsbedenken verbunden sind;
- für andere Verabreichungswege als oral oder topisch, z., zur Verwendung als Injektion oder nasal eingenommen;
- , die behaupten, schwere und/oder lebensbedrohliche Krankheiten und Zustände wie Krebs zu behandeln oder zu verhindern;
- , die an gefährdete Bevölkerungsgruppen, einschließlich Kinder, schwangere Frauen und ältere Menschen, vermarktet werden; oder
- mit erheblichen Qualitätsproblemen.
Wird die FDA homöopathische Produkte vom Markt nehmen?
der FDA oberste Priorität ist die Sicherheit der Patienten. Wenn der Entwurf der Leitlinien fertiggestellt ist, werden die Produktkategorien festgelegt, die die Agentur für die Durchsetzung priorisieren möchte., In der Zwischenzeit beabsichtigt die FDA, vor Abschluss des Entwurfs der Leitlinien ihren allgemeinen Ansatz zur Priorisierung risikobasierter Regulierungs-und Durchsetzungsmaßnahmen anzuwenden.
Schreibe einen Kommentar